薬物動態:肝機能障害者(外国人データ)
薬物動態:肝機能障害者(外国人データ)
1. 単回投与1)
軽度肝機能障害患者(Child-Pughスコア5~6)8例、中等度肝機能障害患者(Child-Pughスコア7~9)8例に、カンサイダス®70mgを60分間かけて単回静脈内投与した。健康成人と比べ、軽度肝機能障害患者ではカンサイダス®のAUC0-∞が約55%、中等度肝機能障害患者では約76%増加した。
■ 軽度及び中等度肝機能障害患者及び健康成人男性にカンサイダス®70mgを単回静脈内投与した時の薬物動態パラメータ(外国人データ)
健康成人男性を対象とした単回投与試験及び健康高齢者を対象とした単回投与試験
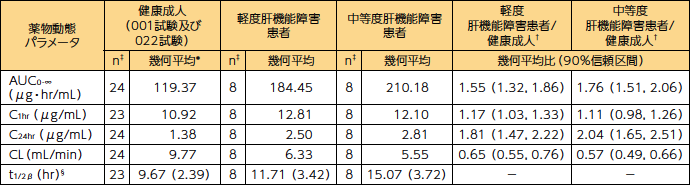
†001試験及び022試験
‡被験者数
§ 調和平均(ジャックナイフ標準偏差)
*これらの平均二乗誤差はAUC0-∞、C1hr、C24hr、CL及びt1/2βでそれぞれ0.05、0.0337、0.0897、0.05及び0.000236であった。
2. 反復投与2)
軽度肝機能障害患者(Child-Pughスコア5~6)8例に、カンサイダス®を投与初日に70mg、第2日~第14日に50mg、中等度肝機能障害患者(Child-Pughスコア7~9)8例には、カンサイダス®を投与初日に70mg、第2日~第14日に35mg、60分間かけて1日1回反復静脈内投与した。軽度肝機能障害患者は、健康成人と比べて、第7日及び第14日のカンサイダス®のAUC0-24hrはそれぞれ約26%、約21%増加し、C1hrは健康成人と同程度であり、C24hrはそれぞれ約70%、約44%増加した。中等度肝機能障害患者では、第7日及び第14日のカンサイダス®のAUC0-24hrは健康成人と同程度であり、C1hrはそれぞれ約20%、約23%減少し、C24hrはそれぞれ約71%、約50%増加した。
■ 軽度及び中等度肝機能障害患者及び健康成人にカンサイダス®70mg(第1日)/50mg又は35mg(第2日~第14日)を反復静脈内投与した時の薬物動態パラメータ(外国人データ)
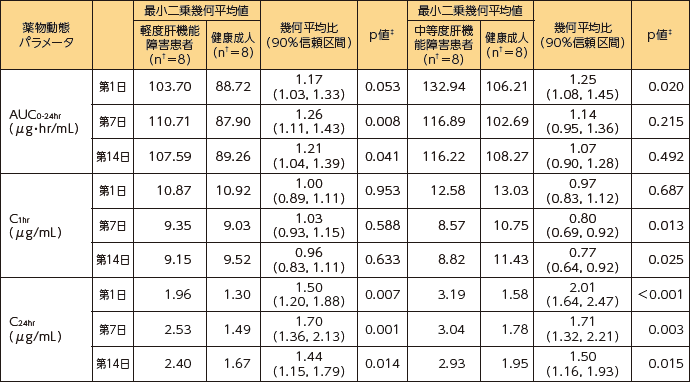
†被験者数
‡p値はそれぞれ軽度及び中等度肝機能障害患者と健康成人の差に対して算出した。
6. 用法及び用量
〈成人〉
真菌感染が疑われる発熱性好中球減少症
通常、カスポファンギンとして投与初日に70mgを、投与2日目以降は50mgを1日1回投与する。本剤は約1時間かけて緩徐に点滴静注する。
カンジダ属又はアスペルギルス属による下記の真菌感染症
・食道カンジダ症
通常、カスポファンギンとして50mgを1日1回投与する。本剤は約1時間かけて緩徐に点滴静注する。
・侵襲性カンジダ症、アスペルギルス症
通常、カスポファンギンとして投与初日に70mgを、投与2日目以降は50mgを1日1回投与する。本剤は約1時間かけて緩徐に点滴静注する。
7. 用法及び用量に関連する注意 −抜粋−
〈成人〉
7.1 中等度の肝機能障害を伴う患者に対しては、下表を目安に本剤の用量調節をすること。[16.6.1参照]

軽度の肝機能障害(Child-Pughスコア5~6)を伴う患者に対しては通常の用量を投与する。
重度の肝機能障害(Child-Pughスコア10以上)を伴う患者に対しては本剤の投与経験がない。
8. 重要な基本的注意
8.1 本剤の投与期間は患者の臨床症状、効果等に基づき決定し、治療上必要な最小限の期間の投与にとどめること。[17.1.1、17.1.2参照]
8.2 肝機能障害があらわれることがあるので、定期的に肝機能検査を行うなど、患者の状態を十分観察すること。[11.1.2参照]
1)社内資料(肝機能障害患者を対象とした海外単回投与試験:009試験)
2)社内資料(肝機能障害患者を対象とした海外反復投与試験:030試験)