有効性:侵襲性カンジダ症患者
有効性:侵襲性カンジダ症患者
海外第Ⅲ相臨床試験成績〈成人〉
侵襲性カンジダ症患者を対象とした海外臨床試験(非劣性試験)1)、2)(海外データ)
1)Mora-Duarte J, et al., N Engl J Med, 2002;347:2020-2029.
(利益相反:MSD社は本試験に資金提供。Rotstein、Colombo、PerfectはMSD社のコンサルタントで、研究助成金や講演料をMSD社から受領。Thompson-Moyaは講演料をMSD社から受領。Smietana、Lupinacci、Sable 、KartsonisはMSD社米国研究所員。)
2)承認時評価資料(侵襲性カンジダ症を対象とした海外臨床試験:014試験)
試験方法

MITT:治験薬の投与を1回以上受け、かつ侵襲性カンジダ症と確定診断された患者
注)本邦において静注として承認されている用法・用量は「通常、成人に対しては、1日体重1kg当りアムホテリシンB0.25mg(力価)より開始し、次回より症状を観察しながら漸増し、1日量として体重1kg当り0.5mg(力価)を点滴静注するが、投与量は1日体重1kg当り1mg(力価)または隔日体重1kg当り1.5mg(力価)までとする。副作用の発現のため投与困難な場合には、初回量は1日1mg(力価)より開始し、症状を観察しながら漸増し、1日総量50mg(力価)までを連日又は隔日1回点滴静注する。点滴静注は3~6時間以上かけて徐々に行う。」である。
有効性
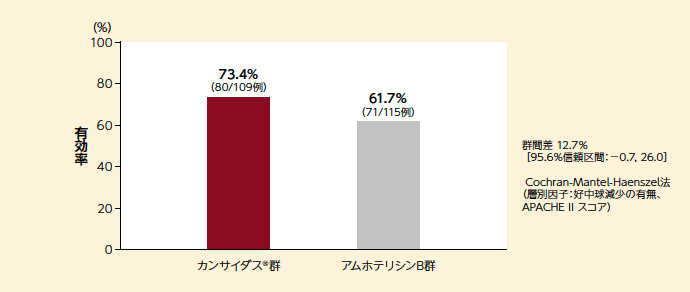
MITT解析による総合効果の有効率は、カンサイダス®群が73.4%(80/109例)、アムホテリシンB群が61.7%(71/115例)であった。有効率の差の推定値は12.7%[95.6%信頼区間:−0.7, 26.0]で、あらかじめ設定した非劣性マージン(95.6%信頼区間が0を含み、下限が−20%を下回らない)を満たしたことから、カンサイダス®のアムホテリシンBに対する非劣性が検証された。カンサイダス®のアムホテリシンBに対する優越性は認められなかった。
■ 総合効果の有効率(MITT、主要評価項目)
安全性
カンサイダス®群の臨床症状の副作用発現率は28.9%(33/114例)であり、主なものは発熱8例(7.0%)、精神神経系7例(6.1%)、悪寒6例(5.3%)、臨床検査値の副作用発現率は24.3%(27/111例)であり、主なものは血清カリウム減少11/111例(9.9%)、血清Al-P増加9/109例(8.3%)、血清直接ビリルビン増加3/79例(3.8%)であった。アムホテリシンB群の臨床症状の副作用発現率は58.4%(73/125例)であり、主なものは悪寒33例(26.4%)、発熱29例(23.2%)、頻脈、頻呼吸各13例(10.4%)、臨床検査値の副作用発現率は54.0%(67/124例)であり、主なものは血清カリウム減少29/124例(23.4%)、血清クレアチニン増加28/124例(22.6%)、血中尿素増加19/120例(15.8%)であった。
臨床症状の重篤な副作用はカンサイダス®群で1例(静脈血栓症)、アムホテリシンB群で16例(急性腎機能不全6例、高血圧4例、気管支収縮、頻脈各2例等)にみられた。臨床検査値の重篤な副作用はカンサイダス®群で発現せず、アムホテリシンB群で2例(血清クレアチニン増加1例、白血球数減少、好中球数減少、血清総ビリルビン増加、AST増加、ALT増加及びAl-P増加1例)にみられた。臨床症状の投与中止に至った副作用はカンサイダス®群で3例(腎機能不全、発熱、呼吸困難各1例)、アムホテリシンB群で21例(急性腎機能不全、腎機能不全各4例、気管支収縮、悪寒、発熱、高血圧、頻脈、発疹各2例等)にみられた。臨床検査値の投与中止に至った副作用はカンサイダス®群で1例(血清クレアチニン増加及び血中尿素窒素増加)、アムホテリシンB群で14例(血清クレアチニン増加10例、AST増加、ALT増加各3例、血中尿素窒素増加2例等)にみられた。副作用による死亡例は、アムホテリシンB群の1例(心停止)のみであった。
5. 効能又は効果に関連する注意 −抜粋−
〈侵襲性カンジダ症〉
5.4 カンジダ血症、腹腔内膿瘍、腹膜炎、胸腔内感染以外における検討は行われていない。[17.1.1、17.1.2 参照]
8. 重要な基本的注意 −抜粋−
8.1 本剤の投与期間は患者の臨床症状、効果等に基づき決定し、治療上必要な最小限の期間の投与にとどめること。[ 17.1.1、17.1.2参照]