海外のHPVワクチンエビデンス
海外のHPVワクチンエビデンス
各国のHPVワクチン接種プログラム
●各国のHPVワクチン接種プログラム
図1は各国のHPVワクチン接種プログラムの開始年、実施法および定期接種コホート、15歳時点の初回接種率についてまとめたものです。
図1:各国のHPVワクチン接種プログラム
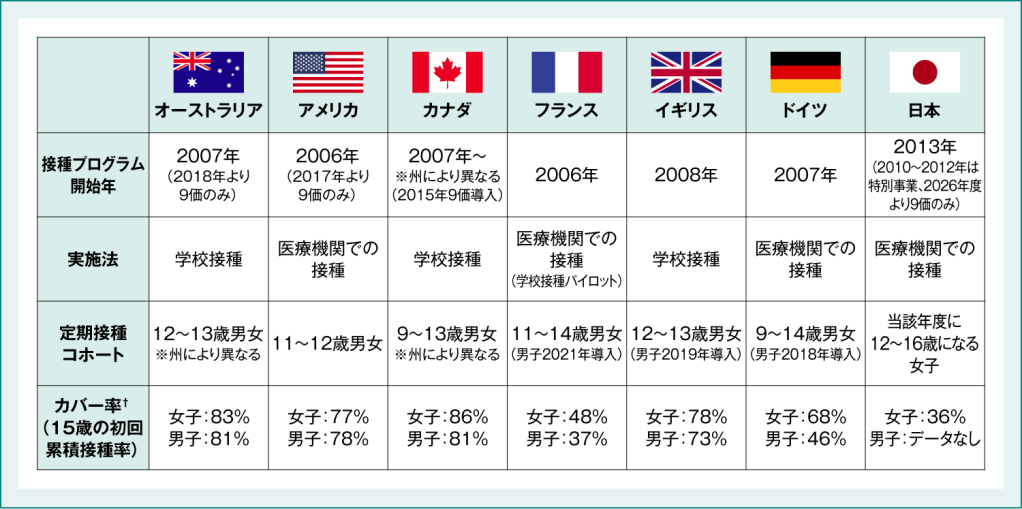
各国の公的機関情報並びにWHO HPV Dashboard(https://www.who.int/teams/immunization-vaccines-and-biologicals/diseases/human-papillomavirus-vaccines-(HPV)/hpv-clearing-house/hpv-dashboard)(Accessed Dec. 12, 2025) より作成。
†:WHO Human papillomavirus(HPV)vaccination coverage
https://immunizationdata.who.int/global/wiise-detail-page/human-papillomavirus-(hpv)-vaccination-coverage(Accessed Dec. 12, 2025)2024年のデータを示した。
日本における9価HPVワクチンの用法及び用量は、9歳以上の者に、1回0.5mLを合計3回、筋肉内に注射する。通常、2回目は初回接種の2ヵ月後、3回目は6ヵ月後に同様の用法で接種する。9歳以上15歳未満の者は、初回接種から6~12ヵ月の間隔を置いた合計2回の接種とすることができる。
子宮頸がんインパクト(スウェーデン)(海外データ)
●ガーダシル®接種と浸潤性子宮頸がんのリスク低下との関連
スウェーデンにおいては、全国的な人口統計および保健に関するレジストリを用いて、10~30歳の女性1,672,983例を対象に、ガーダシル®接種と浸潤性子宮頸がんのリスクとの関連等について検討した結果が報告されました。
ガーダシル®接種群において、非接種群に対するすべての共変量を調整した場合の調整罹患率比は0.37[95%信頼区間(0.21-0.57)]でした。また、17歳未満で接種した場合の調整罹患率比は0.12[95%信頼区間(0.00-0.34)]、17~30歳で接種した場合の調整罹患率比は0.47[95%信頼区間(0.27-0.75)]でした(図2)1)。
浸潤性子宮頸がんの累積罹患率は、ガーダシル®非接種群において、30歳までに10万例あたり94例でした。一方、ガーダシル®接種群においては、17~30歳で接種を開始した女性において、30歳までに10万例あたり54例、17歳未満で接種を開始した女性においては、28歳までに10万例あたり4例と報告されました(図3)1)。
図2:ガーダシル®接種と浸潤性子宮頸がん罹患リスクの低下との関連
図3:ガーダシル®接種の有無と浸潤性子宮頸がんの累積罹患率
【安全性】本論文中に安全性に関する記載はありません。ガーダシル®に関する安全性の詳細につきましては、電子添文をご参照ください。
【対象・方法】2006~2017年の間に、スウェーデンの全国的な人口統計および保健に関するレジストリに登録された、浸潤性子宮頸がんの病歴および本試験の登録前にHPVワクチン接種歴のない10~30歳女性1,672,983例(接種群:527,871例、非接種群:1,145,112例)を対象に、ガーダシル®接種と浸潤性子宮頸がんのリスクとの関連を検討した。1回以上のガーダシル®接種者を接種群(3回接種の割合:56.3%)とした。対象集団のうち、接種群の女性438,939例(83.2%)が17歳未満でガーダシル®の接種を開始した。ガーダシル®の接種状況別の子宮頸がんの累積罹患率については、追跡時の年齢に応じてプロットした。接種群と非接種群の罹患率比およびガーダシル®接種開始時の年齢別の罹患率比については、ポアソン回帰モデルを用いて推定し、年齢、暦年、居住地および親の特性(学歴、世帯収入、母親の出生国、母親の病歴*など)の共変量により調整した(すべて両側検定)。
【Limitation】本研究では、ガーダシル®接種と子宮頸がんのリスクにはいくつかの交絡が確認されている。特にワクチン接種群では、非接種群と比較し、より健康である可能性があった(健康ボランティアバイアス)。著者らは、ワクチン接種と潜在的な子宮頸がんのリスクに影響を与えた親の特性にて調整を行った。しかしながら、女性自身のライフスタイルと健康要因(喫煙状況、性活動、OC**の服用、肥満)による交絡は排除できなかった。また、ワクチン接種群において子宮頸がん検診率が高い場合、無症候性の子宮頸がんが検出される可能性が高くなると推測される。これはリスク低減の過小評価に関連する可能性があると考えられた。
*:過去のCIN3+および子宮頸がん以外のがんの診断
**:低用量経口避妊薬
Lei J et al. N Engl J Med. 2020; 383: 1340-1348.
【利益相反】著者にMSD社より研究助成費を受領している者が含まれる。
4価HPVワクチン(ガーダシル®) の用法及び用量は以下のとおりです。
6. 用法及び用量
9歳以上の者に、1回0.5mLを合計3回、筋肉内に注射する。通常、2回目は初回接種の2ヵ月後、3回目は6ヵ月後に同様の用法で接種する。
7. 用法及び用量に関連する注意
7.1 接種間隔
1年以内に3回の接種を終了することが望ましい。なお、本剤の2回目及び3回目の接種が初回接種の2ヵ月後及び6ヵ月後にできない場合、2回目接種は初回接種から少なくとも1ヵ月以上、3回目接種は2回目接種から少なくとも3ヵ月以上間隔を置いて実施すること。
7.2 同時接種
医師が必要と認めた場合には、他のワクチンと同時に接種することができる。[14.1.1 参照]
参考文献
1) Lei J et al. N Engl J Med. 2020; 383: 1340-1348.