薬物動態:腎機能障害者(外国人データ)
薬物動態:腎機能障害者(外国人データ)1)
1)社内資料(腎機能障害者及び健康被験者を対象とした経口懸濁液の単回投与試験:P01940試験)
ノクサフィル®経口懸濁液*の単回投与後、軽度及び中等度の腎機能障害(12例、クレアチニンクリアランス≧20mL/min/1.73m2)がポサコナゾールの薬物動態に及ぼす影響はみられなかったため、用量調節の必要はないと考えられました。重度腎機能障害者(6例、クレアチニンクリアランス<20mL/min/1.73m2)では、ポサコナゾールのAUCはその他の腎機能障害群(変動係数:≦32%)と比較して大きくばらつきました(変動係数:96%)。ポサコナゾールは血液透析で除去されません。
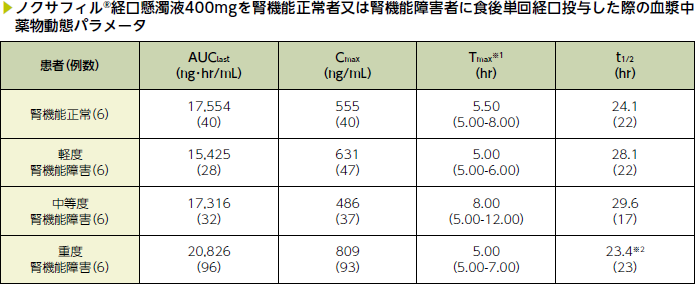
平均値(変動係数%)
※1:中央値(範囲)、※2:4例
*:国内未承認の剤形、用法及び用量
注意:本邦で承認されたノクサフィル®の剤形は錠剤又は静注液です。
6. 用法及び用量
錠100mg
通常、成人にはポサコナゾールとして初日は1回300mgを1日2回、2日目以降は300mgを1日1回経口投与する。
点滴静注300mg
通常、成人にはポサコナゾールとして初日は1回300mgを1日2回、2日目以降は300mgを1日1回、中心静脈ラインから約90分間かけて緩徐に点滴静注する。
9. 特定の背景を有する患者に関する注意 ―抜粋―
9.2 腎機能障害患者
錠100mg
9.2.1 重度(eGFR<20mL/min/1.73m2)の腎機能障害のある患者
本剤の投与中は、真菌症の発症の有無を注意深くモニタリングするなど患者の状態を慎重に観察すること。本剤の曝露量が大きくばらつくおそれがある。[16.6.2参照]
点滴静注300mg
9.2.1 中等度以上(eGFR<50mL/min/1.73m2)の腎機能障害のある患者
治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。投与する場合には血清クレアチニン値を観察し、上昇が認められた場合には錠剤への切り替えを考慮すること。添加剤スルホブチルエーテルβ-シクロデキストリンナトリウムが蓄積し、腎機能障害を悪化させるおそれがある。[7.1参照]
9.2.2 重度(eGFR<20mL/min/1.73m2)の腎機能障害のある患者
本剤の投与中は、真菌症の発症の有無を注意深くモニタリングするなど患者の状態を慎重に観察すること。本剤の曝露量が大きくばらつくおそれがある。[16.6.2参照]
13. 過量投与
ポサコナゾールは血液透析で除去されない。[16.6.2参照]