再接種許可の経緯
再接種が許可されるまでの流れについて
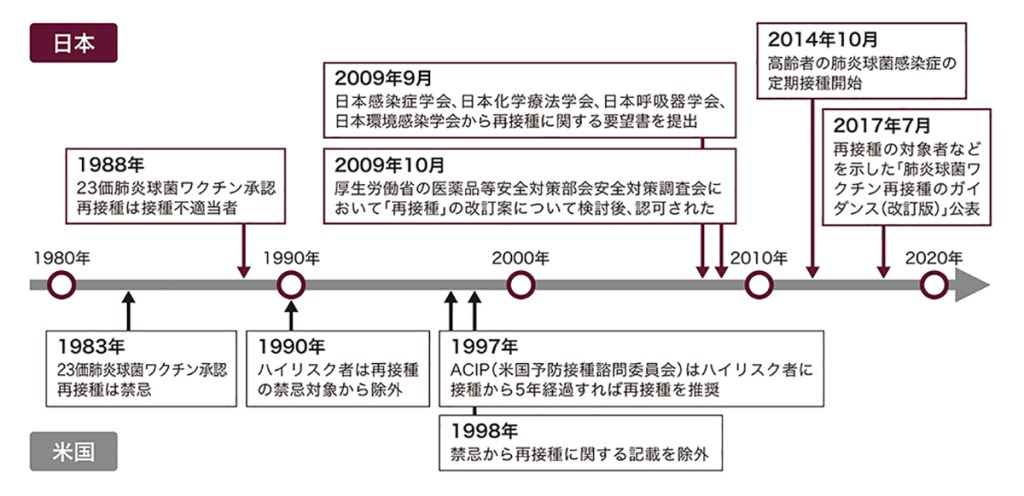
1980年代に23価肺炎球菌ワクチンが承認された際には、多価肺炎球菌莢膜ポリサッカライドワクチンを接種されたことがある者では、局所反応が初回接種時より重症化したとの報告1)があったことから、日米ともに再接種は「禁忌」(日本では「接種不適当者」)とされましたが、その後、接種から4年以上経過すると再接種と有害事象発現率の上昇は関連しないことが示唆された2)ため、米国では再接種は「禁忌」ではなくなりました。
日本では、抗体価を維持するために再接種の必要性が認識されたことなどを背景に、2009年に、23価肺炎球菌ワクチンであるニューモバックス®NPの添付文書が改訂され、再接種は「接種不適当者」から除外されました。2017年には再接種の対象者や注意事項を示した「肺炎球菌ワクチン再接種のガイダンス(改訂版)」が公表されました。
1)Borgono JM, et al. Proc Soc Exp Biol Med. 1978; 157: 148-154.
2)MMWR 1989; 38(5): 64-68, 73-76. https://www.cdc.gov/mmwr/preview/mmwrhtml/00042325.htm(2024/2/26アクセス)
再接種の対象者(「肺炎球菌ワクチン再接種のガイダンス(改訂版)*」より)
初回接種から5年以上経過した者を対象とする(注釈 なお、無脾、脾機能不全の小児及び成人に対して初回接種から5年以上経過している場合接種対象者に含める)。
*:本ガイダンスでは23価肺炎球菌莢膜多糖体ワクチン(23価肺炎球菌ワクチン)の再接種のみ取り扱うこととされている。
一社)日本感染症学会肺炎球菌ワクチン再接種問題検討委員会:感染症学雑誌 2017; 91(4): 543-552.
再接種に関する注意のお願い
ニューモバックス®NPを再接種する際には、前回接種から十分な間隔を確保してください。

