抗体価の変化
国内第Ⅰ相試験 ニューモバックス®NPによる肺炎球菌血清型別抗体価の変化
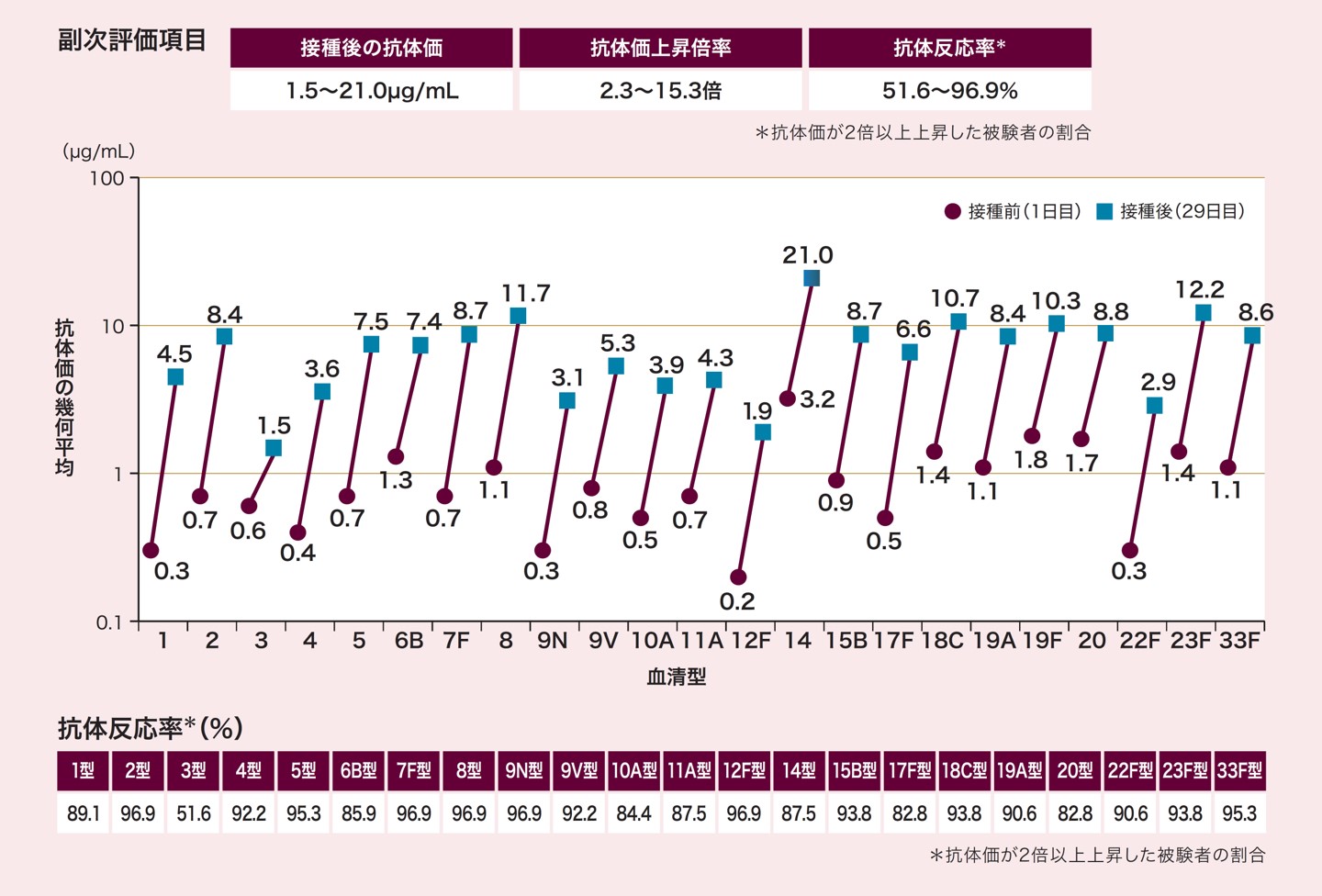
ニューモバックス®NP接種前後の抗体価上昇倍率、肺炎球菌血清型別抗体価、抗体反応率
ニューモバックス®NPに含まれる23種類の血清型別の抗体価は、ニューモバックス®NP接種前は0.2~3.2μg/mL、接種後は1.5~21.0μg/mLでした。
ニューモバックス®NPの安全性
有害事象発現率は75.4%(49/65例)でした。主な有害事象は注射部位疼痛72.3%(47/65例)、注射部位 紅斑26.2%(17/65例)、注射部位腫張23.1%(15/65例)でした。試験期間中に死亡例、重篤な有害事象の発現例、有害事象による中止例は認められませんでした。

主要評価項目の結果:両群の類似性が確認されました。
本試験は、ニューモバックス®(旧製剤)及びニューモバックス®NP(現行製剤)を用いた臨床試験です。
製法変更等に係る承認申請を経て、2006年から現行製剤が販売され、旧製剤は販売中止となりました。
承認時評価資料:国内第Ⅰ相試験
医薬品医療機器総合機構. ニューモバックス®NP審査結果報告書. 平成18年8月31日.より作図
https://www.pmda.go.jp/drugs/2006/P200600040/63015300_21800AMY10131_A100_1.pdf(2026/2/16アクセス)