MSI検査/MMR IHC検査とは
MSI検査/MMR IHC検査:MSI検査/MMR IHC検査とは
監修
埼玉県立がんセンター 腫瘍診断・予防科 科長兼診療部長 赤木 究 先生
東京理科大学大学院 生命科学研究科 生命医科学研究所長 落合 淳志 先生
近年、次世代シークエンサー(NGS)の進歩とともに分子標的薬が次々と開発され、ゲノム異常に応じた治療薬を使用するPrecision Medicineが進展しつつある。同時に個々の患者の治療選択を適切に行うためのコンパニオン診断薬の開発も行われ、承認されるようになってきている。個別化医療やPrecision Medicineはこれからの新しいがん医療の中心であり、そこにコンパニオン診断は不可欠な存在である。これに伴い、病理医、臨床検査技師に求められる役割はますます増加している。病理検体からの適切なコンパニオン診断を行うためには、病理検体の適切な管理が重要な課題である。
また、がん種横断的な治療薬の開発もここ数年注目を集めている。キイトルーダ®は、本邦初のがん種横断的な適応である「がん化学療法後に増悪した進行・再発の高頻度マイクロサテライト不安定性(MSI-High)を有する固形癌(標準的な治療が困難な場合に限る)」(以下、MSI-High固形癌)の承認を2018年12月に取得し、2021年8月には「治癒切除不能な進行・再発の高頻度マイクロサテライト不安定性(MSI-High)を有する結腸・直腸癌」(以下、MSI-High結腸・直腸癌)の適応を取得した。本適応の追加により、大腸癌においては検査実施のタイミングがこれまでより早期になり、検査数も今後、増えてくることが想定される。
キイトルーダ®のMSI-High固形癌及びMSI-High結腸・直腸癌における適応を判定するためのコンパニオン診断薬として承認されているMSI検査キット(FALCO)は、遺伝的多様性(または遺伝子多型)の影響を受けにくい1塩基繰り返しの5マーカーを用いた、腫瘍組織のみでのMSI-High検出を実現した手法である。同じくコンパニオン診断薬として承認されているミスマッチ修復機能欠損検出キット(ロシュ・ダイアグノスティックス)は、4種類のMMRタンパク質の発現を免疫組織化学染色(IHC)により解析を行う手法である。また、2021年6月にはFoundationOne® CDxがんゲノムプロファイリングがMSI-High固形癌の判定補助として利用が可能となり、2022年3月にはGuardant360 CDx がん遺伝子パネルも同適応の判定補助として利用が可能となり、そのほかにも、数種類の医療機器が承認されている*。
当コンテンツでは、MSI検査キット(FALCO)及びミスマッチ修復機能欠損検出キット(ロシュ・ダイアグノスティックス)について病理医、臨床検査技師がdMMR判定検査を適切に行うための必要な情報を概説しており、当コンテンツがdMMR判定検査の理解につながり、実臨床での指針として役立てば幸いである。
*詳細は、以下を参照ください
医薬品医療機器総合機構(PMDA). コンパニオン診断薬等の情報
(https://www.pmda.go.jp/review-services/drug-reviews/review-information/cd/0001.html)
MSI-High/dMMRの概要
 がん種別にみたMSI-High/dMMRの頻度
がん種別にみたMSI-High/dMMRの頻度
32種類の癌患者12,019例を対象とした解析により、24種類の癌においてMSI‑High固形癌が確認されました。割合が高い順に、子宮内膜癌、胃腺癌、小腸癌、結腸・直腸腺癌、子宮頸癌と、多岐にわたる癌の種類の中でも比較的消化器癌、婦人科癌で頻度が高いことが報告されています。
dMMR判定検査(MSI検査/MMR IHC検査)のプロセス
 キイトルーダ®の適応を判定するためのdMMR判定検査のプロセス
キイトルーダ®の適応を判定するためのdMMR判定検査のプロセス
キイトルーダ®の適応※1を判定する目的でdMMR判定検査(MSI検査/MMR IHC検査)を実施する場合、検査に係る情報(検査の目的、方法、費用など)を主治医が患者に説明しカルテに記載することを推奨します。
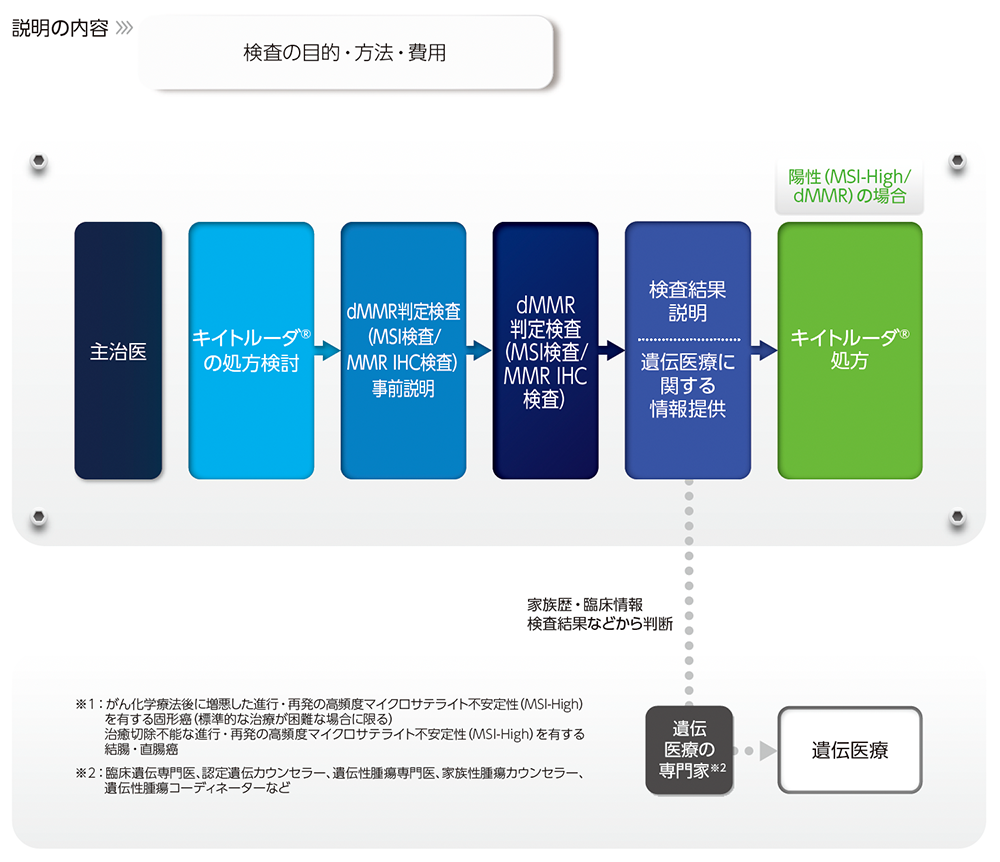
dMMR判定検査とキイトルーダ®の適応
 MSIステータスの判定とキイトルーダ®の適応
MSIステータスの判定とキイトルーダ®の適応
5種類のマイクロサテライト不安定性(MSI)マーカー(BAT‑26、NR‑21、BAT‑25、MONO‑27、NR‑24)の中で、MSI+と識別されたMSIマーカーの数により、以下の判定基準に従ってMSI検査の結果を判定し、キイトルーダ®適応の可否を判断します。
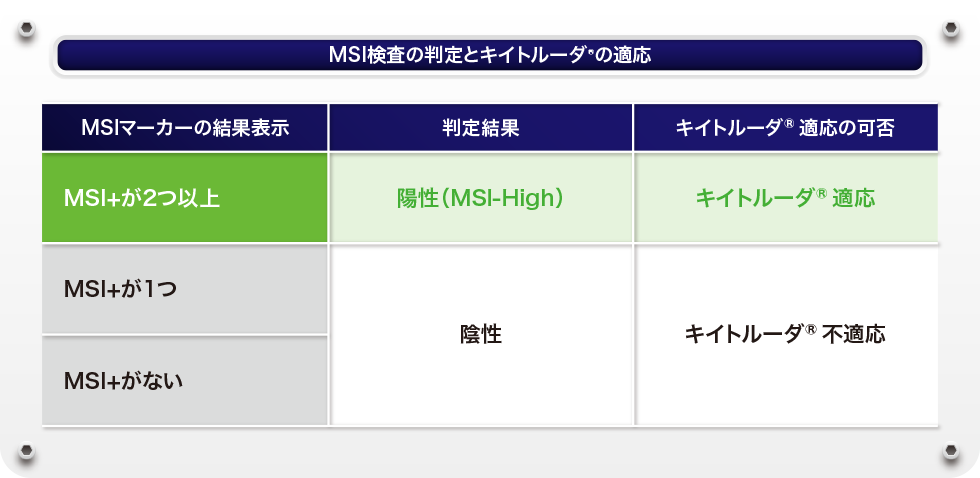
MSI検査キット(FALCO)電子添文第7版より作成
 MMRステータスの判定とキイトルーダ®の適応
MMRステータスの判定とキイトルーダ®の適応
4種類のMMRタンパク質(MLH1、PMS2、MSH2、MSH6)の発現により、dMMRの結果を判定し、キイトルーダ®の適応の可否を判断します。

MSI検査
MSI検査の概要
 MSI検査における保険収載の内容
MSI検査における保険収載の内容
【保険収載の概要】

診療報酬の算定方法の一部を改正する告示(令和6年厚生労働省告示第57号)
診療報酬の算定方法の一部改正に伴う実施上の留意事項について(通知)(令和6年3月5日保医発0305第4号)より改変
 MSI検査フロー
MSI検査フロー
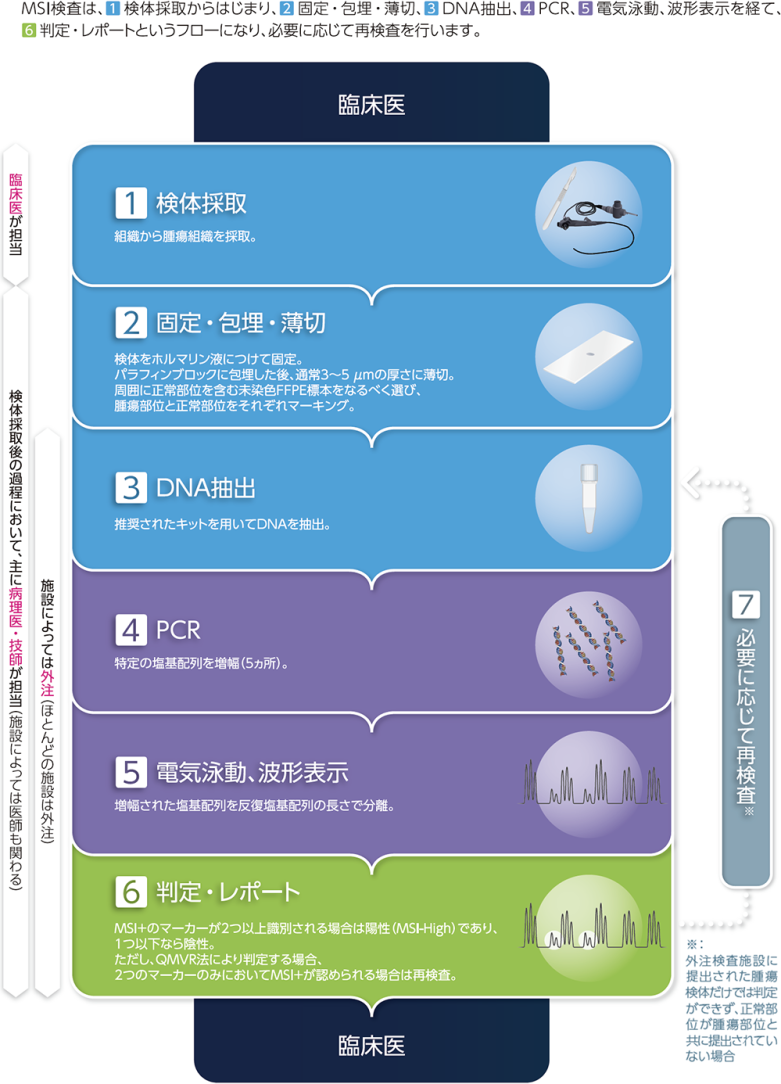
※:外注検査施設に提出された腫瘍検体だけでは判定ができず、正常部位が腫瘍部位と共に提出されていない場合
MSI検査の判定・レポート
 MSI検査の判定
MSI検査の判定

MMR IHC検査
MMR IHC検査の概要
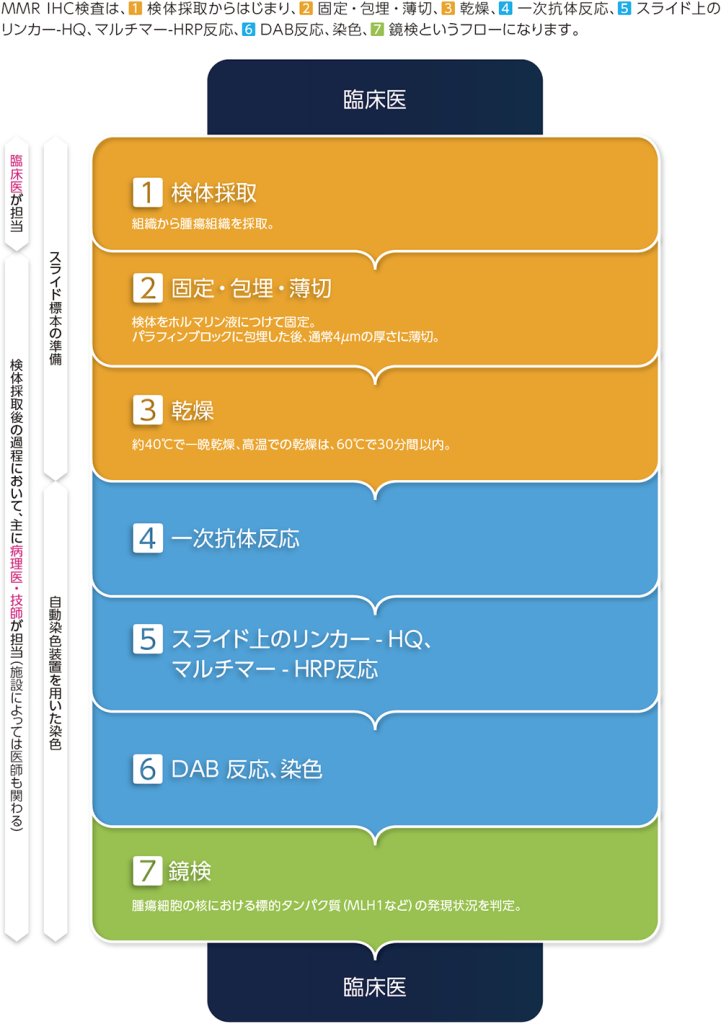
 MMR IHC検査フロー
MMR IHC検査フロー
MMR IHC検査の判定例
 MMR欠損のない大腸癌(pMMR)
MMR欠損のない大腸癌(pMMR)
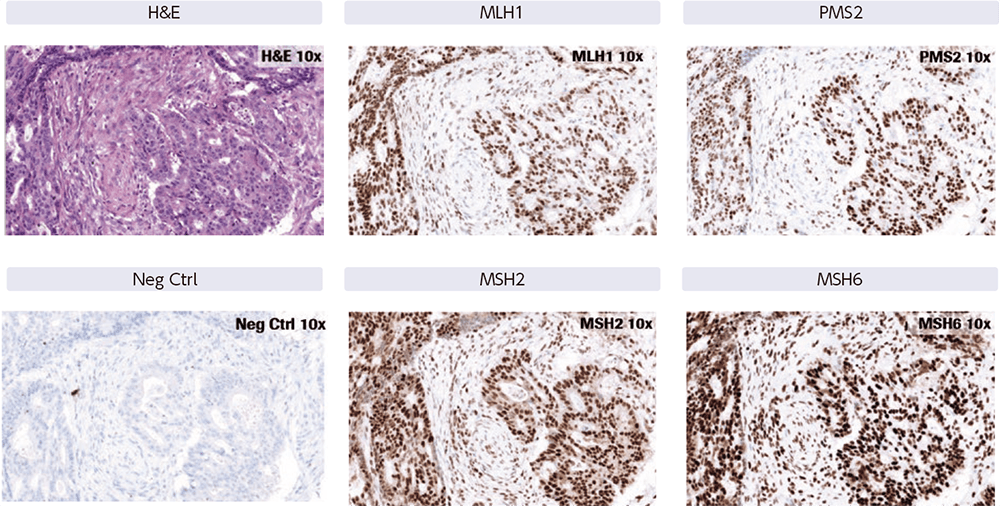
腫瘍細胞・間質の細胞(リンパ球や線維芽細胞など)の核が均一に強陽性を示しました。
 MSH6欠損の大腸癌(dMMR)
MSH6欠損の大腸癌(dMMR)
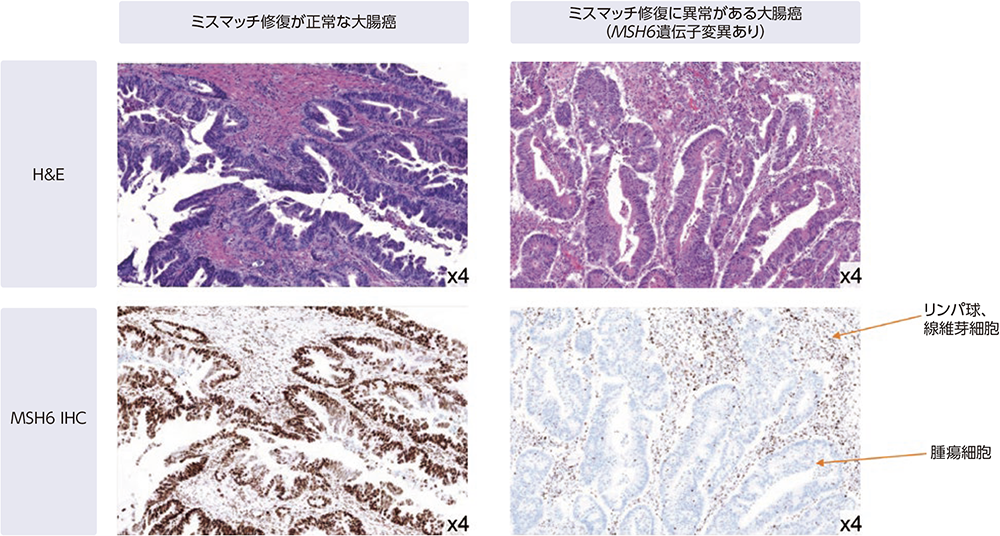
腫瘍細胞の核が陰性化しました。(間質の細胞は陽性)
ロシュ・ダイアグノスティックス提供資料
 ページのTOPへ
ページのTOPへ

