データカットオフ:2017年4月28日
MSI-High固形癌:国際共同臨床試験成績:国際共同第Ⅱ相試験<KEYNOTE-158試験※>
承認時評価資料:国際共同第Ⅱ相試験(KEYNOTE-158試験)
※本試験は、切除不能な局所進行又は転移性の固形癌患者を組み入れたグループA~Kで構成されています。評価資料として審査された、組み入れから27週間以上経過した高頻度マイクロサテライト不安定性(microsatellite instability-high; MSI-High)固形癌患者94例(レトロスペクティブな解析でMSI-Highと判定されたグループA~Jの患者11例及びプロスペクティブな解析でMSI-Highと判定されたグループKの患者83例)の成績についてご紹介します。
<各グループに組み入れられたがん種>
A: 肛門癌(扁平上皮癌)、B: 胆道癌[胆嚢及び胆管の腺癌、ただしファーター膨大部腫瘍を除く]、C: 肺、虫垂、小腸、結腸、直腸及び膵臓由来の神経内分泌腫瘍(高分化型又は中分化型神経内分泌腫瘍)、D: 子宮内膜癌(肉腫又は間葉系腫瘍を除く)、E: 子宮頸癌(扁平上皮癌)、F: 外陰癌(扁平上皮癌)、G: 小細胞肺癌、H: 中皮腫、I: 甲状腺癌、J: 唾液腺癌(肉腫又は間葉系腫瘍を除く)、K: MSI-Highの進行性固形がん(結腸・直腸癌を除く)
試験概要
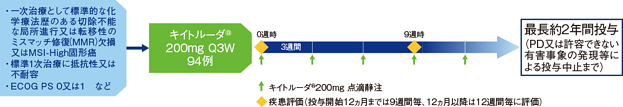
【目的】一次治療として標準的な化学療法歴のある切除不能な局所進行又は転移性のミスマッチ修復(MMR)欠損又はMSI-High*1を有する固形がん患者におけるキイトルーダ®の有効性及び安全性を検討する。
【デザイン】国際共同非無作為化非盲検第Ⅱ相試験
【対象】一次治療として標準的な化学療法歴のある切除不能な局所進行又は転移性のミスマッチ修復(MMR)欠損又はMSI-Highを有する固形癌(non-CRC)患者94例(日本人7例を含む)
【方法】キイトルーダ®200mgを3週間間隔(Q3W)で点滴静注した。投与開始後12ヵ月までは9週間毎、12ヵ月以降は12週間毎に画像検査による評価を行い、疾患進行(PD)又は許容できない有害事象の発現等による投与中止まで、最長約2年間投与を継続した。
【評価項目】主要評価項目:奏効率(overall response rate; ORR)
副次評価項目:奏効期間(duration of response; DOR)、無増悪生存期間(progression free survival; PFS)、全生存期間(overall survival; OS)、安全性
【判定基準】ORR、DOR、PFSは、独立判定委員会(independent review committee; IRC)がRECISTガイドライン1.1版に基づき評価した。
【解析計画】解析対象集団: 有効性*2及び安全性の主要解析はASaT集団*3を対象として実施した。
有効性評価の統計手法: ORRは、点推定値及び二項分布に基づく正確法による95%信頼区間(CI)を算出した。DOR、PFS、OSは、Kaplan-Meier法による生存曲線及びその中央値の推定値を計算した。また、サブグループ解析として、がん種別のORR、DOR、PFS、OSを全体集団と同様の統計手法にて検討した。さらに、日本人集団におけるORR、DOR、PFS、OSは、治験実施計画書に記載されていないが、全体集団と同様の統計手法にて検討し、評価資料として承認時に評価された。
【データカットオフ】 2017年4月28日(承認時評価資料)
*1 本試験ではMMR欠損及びMSI-Highの判定には、それぞれIHC法及びPCR法を用いて検査された
*2 ORRは、全体(グループA~K)及びグループKのASaT集団を対象とした
*3 ASaT(all subjects as treated)集団:治験薬を1回以上投与されたすべての患者
5. 効能又は効果に関連する注意(抜粋)
〈がん化学療法後に増悪した進行・再発のMSI-Highを有する固形癌(標準的な治療が困難な場合に限る)〉
5.8 十分な経験を有する病理医又は検査施設における検査により、MSI-Highが確認された進行・再発の固形癌患者に投与すること。検査にあたっては、関連学会のガイドライン等の最新の情報を参考に、先行の化学療法等によるMSI検査結果への影響及び検査に用いる検体の採取時期について確認し、承認された体外診断用医薬品又は医療機器を用いること。なお、承認された体外診断用医薬品又は医療機器に関する情報については、以下のウェブサイトから入手可能である:
https://www.pmda.go.jp/review-services/drug-reviews/review-information/cd/0001.html
5.9 結腸・直腸癌以外の固形癌の場合、本剤の一次治療における有効性及び安全性は確立していない。また、二次治療において標準的な治療が可能な場合にはこれらの治療を優先すること。
5.10 本剤の手術の補助療法における有効性及び安全性は確立していない。
5.11 臨床試験に組み入れられた患者のがん種等について、「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、本剤以外の治療の実施についても慎重に検討し、適応患者の選択を行うこと。[17.1.14、17.1.15参照]
患者背景(ASaT集団)
*1 陽性(MSI-High)の定義は以下の通りとする
・MSI検査において、MSIマーカー5つのうち、2つ以上のマーカーがMSI+を示した場合
・IHC検査において、MMRタンパク質(MLH1、MSH2、MSH6、PMS2)の発現が1つ以上欠損している場合
*2 RECISTガイドライン1.1版に基づくIRCによる評価
主要評価項目 奏効率:ORR
奏効率(ORR)(ASaT集団)

*1 プロスペクティブな解析でMSI-Highと判定された進行性固形癌(結腸・直腸癌を除く)
*2 日本人3例を含む
*3 二項分布の確率計算による正確法
(追跡期間中央値:8.4ヵ月、範囲:0.6, 14.9)
がん種別の奏効(CR+PR)例数(ASaT集団)(サブグループ解析)
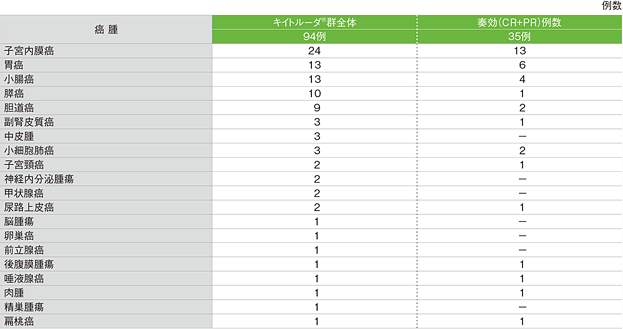
(追跡期間中央値:8.4ヵ月、範囲:0.6, 14.9)
ベースラインからの腫瘍径の最大変化率(ウォーターフォールプロット)(ASaT集団)*
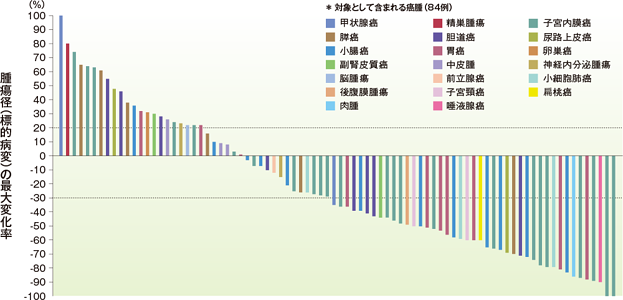
RECISTガイドライン1.1版に基づくIRCによる評価
治験薬投与後に少なくとも1回の画像評価を実施した患者84例の腫瘍径の最大変化率を表示
(追跡期間中央値:8.4ヵ月、範囲:0.6, 14.9)
*1 プロスペクティブな解析でMSI-Highと判定された進行性固形癌(結腸・直腸癌を除く)
*2 治験薬投与後に少なくとも1回の画像評価を実施した患者
副次評価項目 奏効期間:DOR
奏効までの期間及び奏効期間(DOR)の要約(ASaT集団)
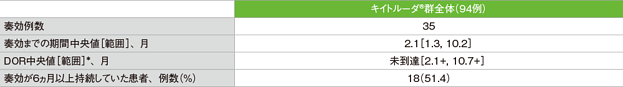
*「+」は最後の疾患評価までにPDがみられないことを示す
(追跡期間中央値:8.4ヵ月、範囲:0.6, 14.9)
- 奏効までの期間中央値は2.1ヵ月(範囲:1.3, 10.2)、DORは中央値に未到達(範囲:2.1+, 10.7+)でした。奏効が認められた患者35例のうち、奏効が6ヵ月以上持続していた患者は18例(51.4%)でした。
副次評価項目 無増悪生存期間:PFS
無増悪生存期間(PFS)のKaplan-Meier曲線(ASaT集団)
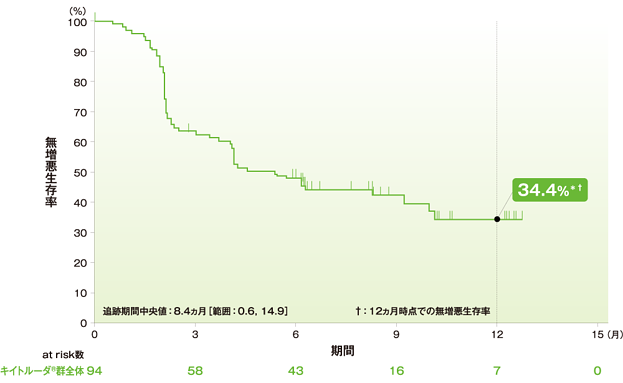
無増悪生存期間(PFS)の要約(ASaT集団)
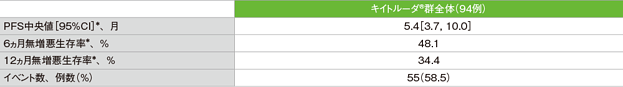
*打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:8.4ヵ月、範囲:0.6, 14.9)
- PFS中央値は5.4ヵ月(95%CI:3.7, 10.0)でした。6ヵ月無増悪生存率は48.1%、12ヵ月無増悪生存率は34.4%でした。
副次評価項目 全生存期間:OS
全生存期間(OS)のKaplan-Meier曲線(ASaT集団)
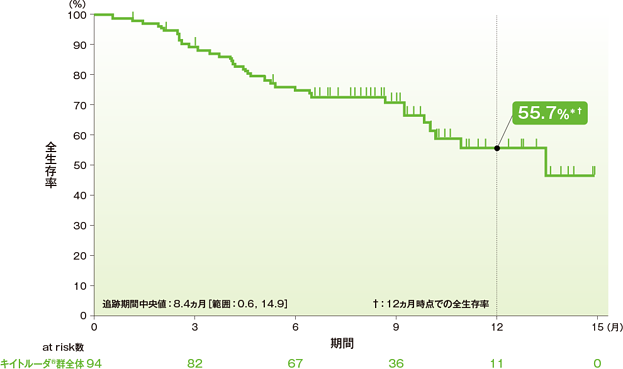
全生存期間(OS)の要約(ASaT集団)
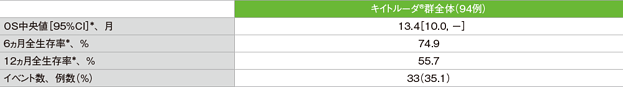
*打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:8.4ヵ月、範囲:0.6, 14.9)
- OS中央値は13.4ヵ月(95%CI:10.0, 未到達)でした。6ヵ月全生存率は74.9%、12ヵ月全生存率は55.7%でした。
安全性
副作用は58/94例(61.7%)に認められました。主な副作用(発現率10%以上)は、そう痒症、疲労各11例(11.7%)でした。重篤な副作用は7例(7.4%)に認められ、その内訳は肺臓炎2例(2.1%)、甲状腺機能亢進症、下痢、肝酵素上昇、劇症1型糖尿病、ギラン・バレー症候群各1例(1.1%)でした。副作用による中止は6例(6.4%)に認められ、その内訳は血中アルカリホスファターゼ増加2例(2.1%)、肺臓炎、γ-グルタミルトランスフェラーゼ増加、ヘモグロビン減少、肝酵素上昇、肝機能検査値上昇、ギラン・バレー症候群各1例(1.1%)でした。副作用による死亡は認められませんでした。
副作用(発現率5%以上)(ASaT集団)
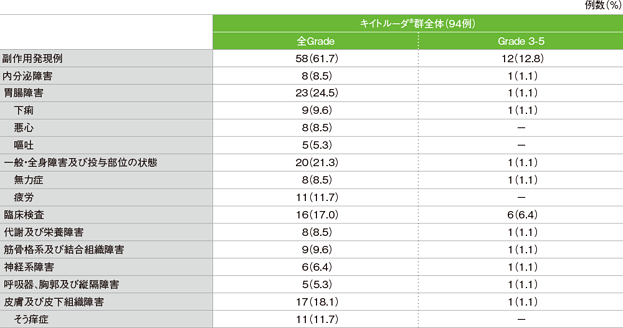
MedDRA/J v20.0、GradeはCTCAE v4.0
免疫関連など特に注目すべき有害事象
免疫関連など特に注目すべき有害事象は17/94例(18.1%)に認められました。主な免疫関連など特に注目すべき有害事象(発現率5%以上)は、甲状腺機能低下症5例(5.3%)でした。重篤な免疫関連など特に注目すべき有害事象は5例(5.3%)に認められ、その内訳は肺臓炎2例(2.1%)、甲状腺機能亢進症、ギラン・バレー症候群、劇症1型糖尿病各1例(1.1%)でした。起因する中止は2例(2.1%)に認められ、その内訳はギラン・バレー症候群、肺臓炎各1例(2.1%)でした。起因する死亡は認められませんでした。
免疫関連など特に注目すべき有害事象(ASaT集団)
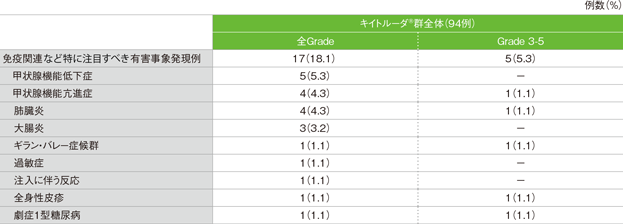
MedDRA/J v20.0、GradeはCTCAE v4.0


