BENCHMRK-1、BENCHMRK-2試験
BENCHMRK-1、BENCHMRK-2試験
抗HIV治療経験のあるHIV感染者を対象にした第Ⅲ相臨床試験(BENCHMRK 1、BENCHMRK 2試験注))(海外データ)1)~3)
1)承認時評価資料(海外第Ⅲ相試験:BENCHMRK1及び2)
2)Steigbigel RT, et al. N Engl J Med 2008;359(4):339-354.
(利益相反:Merck & Co., Inc., Rahway, N.J., U.S.A.が本試験に資金提供。Steigbigel、LoutfyはMerck & Co., Inc., Rahway, N.J., U.S.A.の委託研究者。Cooperは講師料、アドバイザー料を受領。Kumar、Clotetはコンサルタント料、講師料を受領。Eron、Schechterはコンサルタント料または講師料を受領。Markowitzはコンサルタント料、助成金を受領。Lennoxはコンサルタント料を受領。Gatellは助成金または講師料またはアドバイザー料を受領。Rockstroh、Katlamaは講師料またはアドバイザー料を受領。Yeniは助成金、アドバイザー料を受領。Lazzarinはアドバイザー料、コンサルタント料、講師料を受領。Zhao、Chen、Meibohm、Miller、Hazuda, DiNubile、Isaacs、Nguyen、Teppler、Mr. Ryan、Rhodes、Killar、Gilde、Strohmaier、NesslyはMerck & Co., Inc., Rahway, N.J., U.S.A.米国研究所員。)
3)Steigbigel RT, et al. Clin Infect Dis 2010;50(4):605-612.
(利益相反:Merck & Co., Inc., Rahway, N.J., U.S.A.が本試験に資金提供。Steigbigel、Cooper、Kumar、Eron、Schechter、Markowitz、Loutfy、Lennox、ClotetはMerck & Co., Inc., Rahway, N.J., U.S.A.の委託研究者。Steigbigel 、Cooper、Kumar、Eron、Schechter、Markowitz、Lennox、Gatell、Rockstroh、Katlama、Yeni 、Lazzarin、ClotetはMerck & Co., Inc., Rahway, N.J., U.S.A.から講師料、アドバイザー料またはコンサルタント料を受領。Cooper、Eron、Markowitz、Loutfy、Gatell、Lennox、Yeni、LazzarinはMerck & Co., Inc., Rahway, N.J., U.S.A.から研究助成を受けた。Zhao、Chen、Meibohm、Miller、Hazuda、DiNubile、Isaacs、Nguyen、Teppler、Ryan、Rhodes、Killar、Gilde、Strohmaier、Nessly、BarnardはMerck & Co., Inc., Rahway, N.J., U.S.A.米国研究所員。)
[目 的]
対象におけるアイセントレス®(400mg 1日2回)のウイルス学的及び免疫学的効果、安全性を検討する。
[試験デザイン]
多施設共同、無作為化、二重盲検、プラセボ対照非劣性検証試験
[対 象]
HIV感染者で、3クラスの抗HIV薬[核酸系逆転写酵素阻害剤(NRTI)、非核酸系逆転写酵素阻害剤(NNRTI)、プロテアーゼ阻害剤(PI)]の各々で1剤以上に耐性が確認され、血漿中HIV RNA量が1,000copies/mL以上である16歳以上の699例
[方 法]
アイセントレス®(400mg 1日2回)と最適基礎療法*1) OBT:optimized background therapy)又はプラセボとOBTのいずれかを96週間投与した。無作為化では、プロテアーゼ阻害剤に対する薬剤耐性の程度(1剤又は2剤以上)及びOBTでのenfuvirtide*2)使用の有無によって層別化した。OBTは、無作為化前に、薬剤耐性検査(遺伝子型解析/表現型解析)及び抗HIV治療歴に基づいて治験責任医師が選択した。
[評価項目]
主要評価項目:16週時における血漿中HIV RNA量<400copies/mLの患者の割合(検証的解析項目)
安全性評価
副次評価項目:各時点(2, 4, 8, 12, 16, 24, 32, 40, 48, 60, 72, 84, 96週時)における血漿中HIV RNA量
<50copies/mLの患者の割合
48, 96週時におけるHIV RNA量<400copies/mLの患者の割合
16, 48, 96週時における血漿中HIV RNA量(Log10 copies/mL)のベースラインからの平均変化量
48, 96週時におけるHIV RNA量>1Log10 copies/mLの低下(drop)又はHIV RNA量<400copies/mLの患者の割合
16, 48, 96週におけるCD4陽性リンパ球数(cells/mm3)のベースラインからの平均変化量
ウイルス学的失敗 など
[解析計画]
主要評価項目である16週時における血漿中HIV RNA量<400 copies/mLの患者の割合については、ベースラインの血漿中HIV RNA量、enfuvirtide未治療患者のOBTにおけるenfuvirtideの使用有無、表現型薬剤耐性検査により決定されたOBTにおける既承認PIの使用有無、darunavir未治療患者のOBTにおけるdarunavirの使用有無、試験及び治療群を共変量としたロジスティック回帰分析によりオッズ比(95%信頼区間)とP値を算出した。オッズ比の95%信頼区間の下限値が1を超える場合に優越性ありと判定した。副次評価項目である16週における血漿中HIV RNA量(Log10 copies/mL)のベースラインからの平均変化量及び CD4陽性リンパ球数のベースラインからの平均変化量については、記述統計量を要約した。両側検定のP値がP<0.05のとき群間に有意差ありとした。
注)BENCHMRK:Blocking integrase in treatment Experienced patients with a Novel Compound against HIV:Merck. MK-0518
BENCHMRK 1及びBENCHMRK 2試験の試験デザインは同一であり、参加国が異なる。
BENCHMRK 1(350例):ヨーロッパ、アジア/太平洋沿岸諸国、ペルー
BENCHMRK 2(349例):南北アメリカ
※本試験計画時のもの
*1)最適基礎療法:薬剤耐性検査及び抗HIV治療歴に基づいて治験責任医師が無作為化前に選択した、患者ごとの抗HIV薬の最適組み合せ療法
*2)国内未承認薬ですが、承認時評価資料であることからデータを掲載しています。
[有効性]
主要評価項目である16週時における血漿中HIV RNA量<400copies/mLの患者の割合は、アイセントレス®群において77.3%( 355/459 例)、プラセボ投与群において41.8%( 99/237例)であり、ロジスティック回帰分析により算出したオッズ比の95%信頼区間の下限値が5.60と、1を上回ったことから、アイセントレス®群のプラセボ投与群に対する優越性が検証されました。※1
副次評価項目である16週時における血漿中HIV RNA量のベースラインからの平均変化量は、アイセントレス®群及びプラセボ投与群においてそれぞれ-1.88 、-0.92 Log10 copies/mLでした。※2
また、16週におけるCD4陽性リンパ球数のベースラインからの平均変化量は、アイセントレス®群及びプラセボ投与群においてそれぞれ+83.86 、+35.58cells/mm3でした。※2
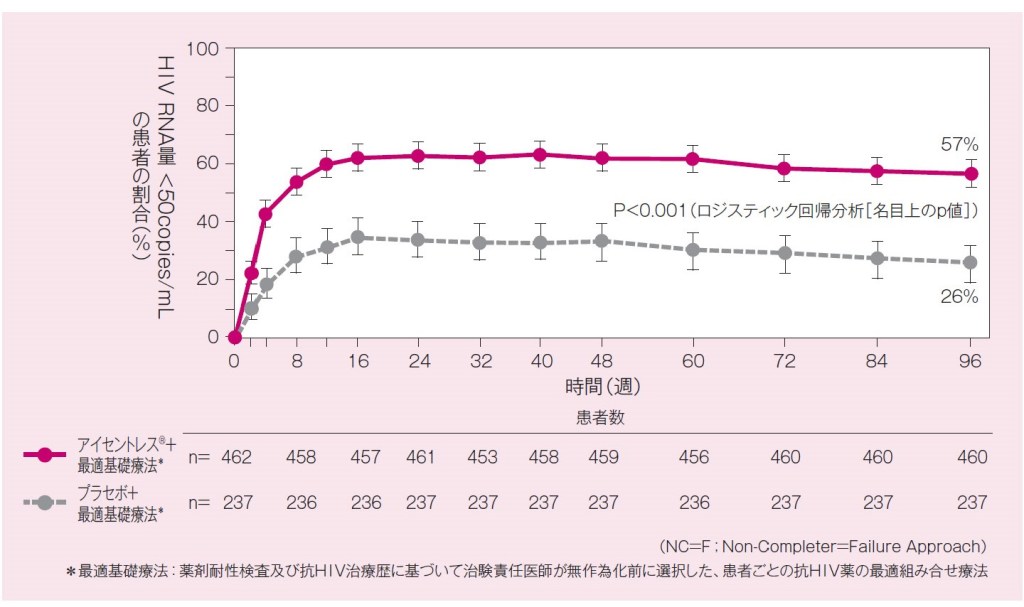
各時点(2, 4, 8, 12, 16, 24, 32, 40, 48, 60, 72, 84, 96週時)における血漿中HIV RNA量<50 copies/mLの患者の割合は図のように推移しました。96週時における血漿中HIV RNA量<50 copies/mLの患者の割合は、アイセントレス® 投与群では57%、プラセボ投与群では26%でした(ロジスティック回帰分析、P<0.001[名目上のp値])。※3
※1 未完了例=失敗例とした。ただし、規定した評価時点のデータが欠測であっても、その前後の来院ともHIV RNA量が<400copies/mL、又はHIV RNA量が<50copies/mLの場合は、当該欠測値を解析から除外した。
※2 効果不十分のために割り付けられた治療を中止した患者では、ベースライン値を評価値として扱うObserved Failure法を採用した(Observed Failure法:効果不十分による中止例=失敗例)。
※3 未完了例=失敗例とした。
BENCHMRK 1試験とBENCHMRK 2試験の併合データ:
投与群別の転帰(48 週時及び96 週時)(主要/副次評価項目)
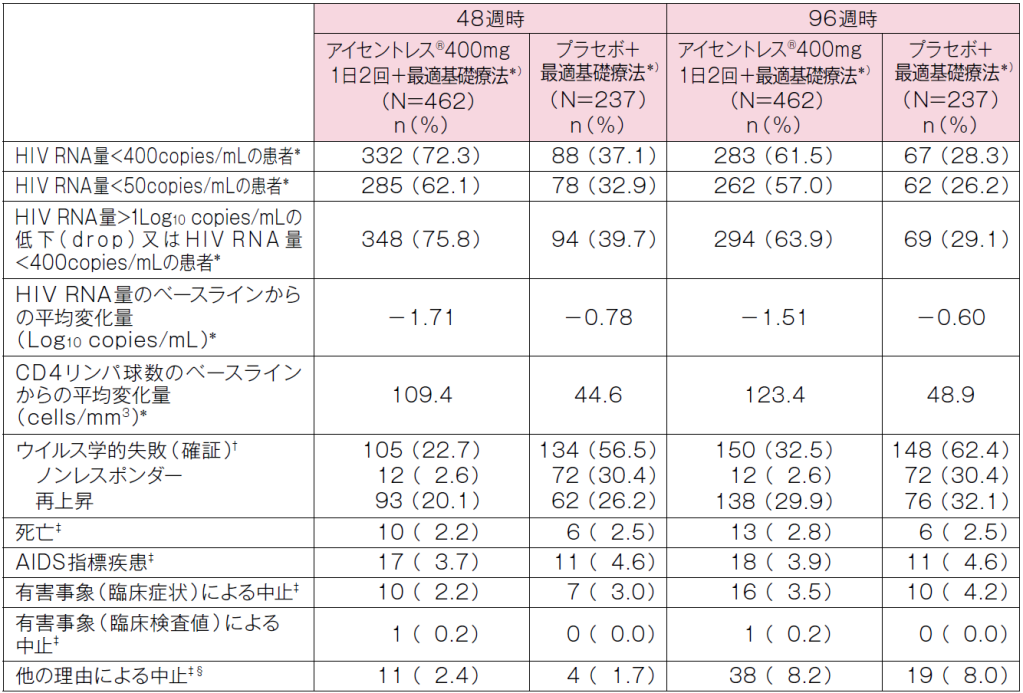
* 欠測値の取扱い方法:二者択一で評価を行う項目(患者割合の評価)については、未完了例=失敗例とした。ただし、規定した評価時点のデータが欠測であっても、その前後の来院ともHIV RNA量が<400copies/mL、又はHIV RNA量が<50copies/mLの場合は、当該欠測値を解析から除外した。HIV RNA量(Log10 copies/mL)のベースラインからの変化量及びCD4リンパ球数のベースラインからの変化量については、効果不十分のために割り付けられた治療を中止した患者では、ベースライン値を評価値として扱うObserved Failure法を採用した(Observed Failure法:効果不十分による中止例=失敗例)。
† ウイルス学的失敗:第16週時までにHIV RNA量が>1.0Log10 copies/mLの低下をしなかった患者、又はHIV RNA量が<400copies/mLに達しなかった患者をノンレスポンダーと定義した。またウイルス量の再上昇は、1週間以上の間隔で2回連続的に行った測定において、(a)HIV RNA量がいったん<400copies/mLに到達後、>400copies/mLに上昇した患者又は(b)HIV RNA量がいったん到達した最低レベルより>1.0Log10 copies/mLの再増加をした患者をリバウンダーと定義した。
‡ 48週時の結果は最低48週時のデータを含む。96週時の結果は、96週までのデータを含む。
§ 追跡不能、同意の撤回、服薬不良、治験実施計画書からの逸脱、その他の理由を含む。
N=各投与群の患者数
BENCHMRK 1試験とBENCHMRK 2試験の併合データ:
血漿中HIV RNA量<50copies/mLの患者の割合の推移(95%信頼区間)
(未完了例=失敗例;NC=F法)(副次評価項目)
[安全性]
96週までの副作用発現率は、アイセントレス® 投与群で58 .4%(270/462 例)、プラセボ投与群で58 .6%(139/237例)でした。アイセントレス®投与群の主な副作用(発現率≧2%)は、頭痛22例(4.8%)、悪心19例(4.1%)、下痢15例(3.2%)、疲労15例(3.2%)、腹部膨満感10例(2.2%)でした。プラセボ投与群の主な副作用は、頭痛12例(5. 1%)、下痢12例(5. 1%)、悪心11例(4. 6%)、発熱6例(2. 5%)、嘔吐5例(2. 1%)でした。
重篤な副作用は、アイセントレス®投与群13例で中毒性腎炎、陰部ヘルペス、慢性腎不全、腎尿細管壊死、薬物性過敏症、急性腎不全、好中球減少症、腎不全及び偶発的過量投与が各1件、心筋梗塞、肝炎、胃炎及び貧血が各2件、過敏症が3件、プラセボ投与群9例で中毒性肝炎、エイズ関連認知症症候群、基底細胞癌、扁平上皮癌、悪性リンパ腫、高血糖症、腎不全、腎結石症、膵炎、好中球減少症及び赤血球形成不全が各1件でした。試験薬の投与中止に至った副作用は、アイセントレス® 投与群6例で肝炎、肝腫大、高乳酸血症、腎不全、注射部位過敏症、注射部位反応及び鼓腸が各1件、プラセボ投与群2例で悪心及び赤血球形成不全が各1件でした。なお、試験期間中にアイセントレス®投与群で13例、プラセボ投与群で7例の患者が死亡し、うちプラセボ投与群の2例(エイズ関連認知症症候群及び悪性リンパ腫が各1件)において薬剤との関連が認められました。