レカルブリオ®に関する過去のお知らせ一覧
過去のお知らせ一覧
本剤の電子添文には、以下のとおり記載されています。
4. 効能又は効果
<適応菌種>
本剤に感性の大腸菌、シトロバクター属、クレブシエラ属、エンテロバクター属、セラチア属、緑膿菌、アシネトバクター属
ただし、カルバペネム系抗菌薬に耐性を示す菌株に限る
<適応症>
各種感染症
5. 効能又は効果に関連する注意
5.1 本剤は、AmblerクラスA又はクラスCのβ-ラクタマーゼの関与が考えられる原因菌による感染症に投与すること。[18.1、18.2.2参照]
5.2 髄膜炎患者での安全性及び有効性は検討されていない。
<引用>
電子添文
レレバクタムはAmblerクラスA及びクラスCのβ-ラクタマーゼを阻害し、イミペネムがこれらの酵素により加水分解されるのを防ぎます。イミペネムはカルバペネム系抗菌薬であり、細菌のペニシリン結合蛋白質に作用し、細胞壁合成を阻害することで殺菌作用を示します。シラスタチンは腎臓におけるイミペネムの代謝・不活性化及び動物実験でみられるイミペネムの腎毒性を抑制します。なお、レレバクタム及びシラスタチンに抗菌活性は認められません。
<引用>
電子添文
本剤の電子添文には、以下のとおり記載されています。
6. 用法及び用量
通常、成人には1回1.25g(レレバクタムとして250mg/イミペネムとして500mg/シラスタチンとして500mg)を1日4回30分かけて点滴静注する。
7. 用法及び用量に関連する注意
7.1 腎機能障害のある患者[クレアチニンクリアランス(CLCR)が90mL/min未満]に対しては下表を参考に本剤の用量を調節すること。また、腎機能が変動している患者では、CLCRを確認すること。[9.2、16.6.1参照]
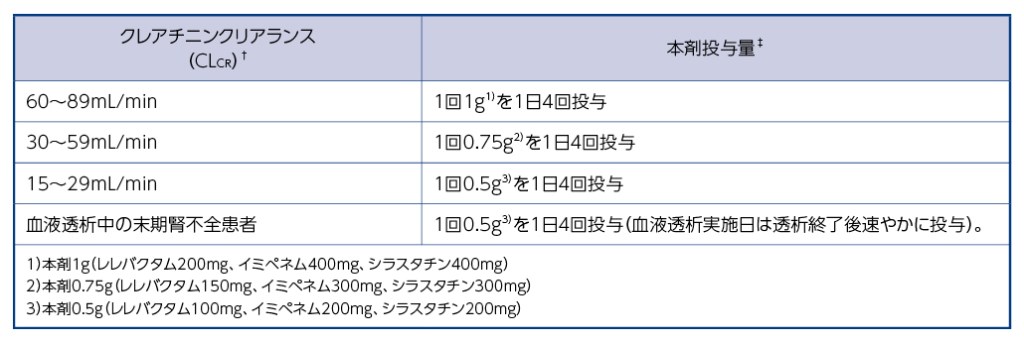
† Cockcroft-Gault式により推定したCLCR
‡ いずれの用量も30分かけて投与する。
7.2 CLCRが15mL/min未満で血液透析をしていない患者における臨床推奨用量の根拠となるデータは得られていない。
<引用>
電子添文
本剤の電子添文には、以下のとおり記載されています。
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 他のβ-ラクタム系抗生物質に対し重篤な過敏症(アナフィラキシー等の重度の全身性アレルギー反応)の既往歴のある患者
2.3 バルプロ酸ナトリウム投与中の患者[10.1参照]
<引用>
電子添文
本剤の電子添文には、以下のとおり記載されています。
9.8 高齢者
腎機能等、患者の状態を観察しながら慎重に投与すること。生理機能が低下している高齢者では副作用があらわれやすい。本剤は腎排泄型の薬剤である。なお、他の抗生物質(セフェム系、アミノグリコシド系等)を投与した高齢者において、ビタミンK欠乏による出血傾向があらわれたとの報告がある。[16.6.3参照]
<引用>
電子添文
本剤の電子添文には、以下のとおり記載されています。
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。イミペネム及びシラスタチンはヒト母乳中へ移行することがある。レレバクタムはラットの母乳中へ移行することが報告されているが、ヒト母乳中へ移行するかどうかは不明である。
<引用>
電子添文
本剤の電子添文には、以下のとおり記載されています。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
<引用>
電子添文
レレバクタム、イミペネム及びシラスタチンは血液透析で除去されますが、過量投与に対する血液透析の有用性は不明です(1)。
なお、血液透析中の末期腎不全患者にレレバクタムとイミペネム・シラスタチンを併用し単回点滴静注した臨床薬理試験では、レレバクタム 67~87%、イミペネム 66~87%、シラスタチン 46~56% が血液透析により除去されました(2)。
<引用>
(1)電子添文
(2)インタビューフォーム Ⅶ. 薬物動態に関する項目
本剤の電子添文には、以下のとおり記載されています。
8. 重要な基本的注意
8.1 本剤の使用は、感染症の治療に十分な知識と経験を持つ医師又はその指導の下で行うこと。
8.2 本剤によるショック、アナフィラキシーの発生を確実に予知できる方法がないので、次の措置をとること。[11.1.2参照]
8.2.1 事前に既往歴等について十分な問診を行うこと。なお、抗生物質等によるアレルギー歴は必ず確認すること。[9.1.1、9.1.2参照]
8.2.2 投与に際しては、必ずショック等に対する救急処置のとれる準備をしておくこと。
8.2.3 投与開始から投与終了後まで、患者を安静の状態に保たせ、十分な観察を行うこと。特に、投与開始直後は注意深く観察すること。
8.3 本剤の使用にあたっては、耐性菌の発現を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
8.4 重篤な肝障害があらわれることがあるので、定期的に検査を実施するなど観察を十分に行うこと。[11.1.4参照]
8.5 重篤な血液障害があらわれることがあるので、定期的に検査を実施するなど観察を十分に行うこと。[11.1.6参照]
8.6 重篤な腎障害があらわれることがあるので、定期的に検査を実施するなど観察を十分に行うこと。[11.1.7参照]
<引用>
電子添文
院内肺炎又は人工呼吸器関連肺炎、複雑性腹腔内感染症又は複雑性尿路感染症のイミペネム耐性菌(中等度耐性を含む)感染症患者を対象とした国際共同第Ⅲ相臨床試験において、本剤を投与された安全性解析対象例31例中5例(16.1%)に副作用が認められました。
認められたすべての副作用は、腎クレアチニン・クリアランス減少2例(6.5%)、注入部位紅斑1例(3.2%)、発熱1例(3.2%)及び高血糖1例(3.2%)でした。
<引用>
電子添文
貯法は、室温保存です。
光を避けるため、箱のまま保存してください。
<引用>
電子添文
投与期間に関して明確な制限はありません。
電子添文の「8. 重要な基本的注意」に一般的な注意として以下のように記載されています。
8.3 本剤の使用にあたっては、耐性菌の発現を防ぐため、原則として感受性を確認し、疾病の治療上必要な最小限の期間の投与にとどめること。
<引用>
電子添文
このサイトでは、医療用医薬品を適正にご使用いただくため、医師、歯科医師及び薬剤師などの医療関係者の方を対象に、主としてMSD株式会社の医療用医薬品に関する情報を提供しています。
下記の「はい」をクリックした場合、「MSD Connect ご利用規約」及び「ウェブサイトのご利用条件」を理解したうえで、内容に同意したものとみなします。
2024年11月にご利用規約を改訂致しました。上記リンクよりご確認ください。
あなたは医療関係者ですか?