DRIVE-FORWARD試験
本剤は海外での臨床試験成績をもとに承認されたため、国内での臨床試験は実施していません。
DRIVE-FORWARD試験
治療未経験のHIV-1感染症患者を対象とした海外第Ⅲ相二重盲検比較試験(海外データ)1)2)
1)Molina JM, et al. Lancet HIV 2018;5(5):e211-e220
(利益相反:Merck & Co., Inc., Rahway, N.J., U.S.A.が資金提供。共著者のLai、Xu、Rodgers、Lupinacci、Kumar、
Sklar、Nguyen、Hanna、HwangはMerck & Co., Inc., Rahway, N.J., U.S.A.の社員。)
2)承認時評価資料(海外第Ⅲ相試験:DRIVE-FORWARD試験)
[目的]
治療未経験のHIV-1感染症患者を対象に、2種類のヌクレオシド系逆転写酵素阻害剤(NRTI)を背景治療として、ピフェルトロ®錠100mgを併用したときの有効性を、ダルナビル+リトナビル(DRV/r)併用と比較検証し、あわせて安全性を検討する。
[試験デザイン]
多施設共同、無作為化、二重盲検、実薬対照第Ⅲ相、非劣性検証試験

[対象]
治療未経験の18歳以上のHIV-1感染症患者(HIV-1 RNA量≥1,000copies/mL)766例(試験薬投与例)
[方法]
対象患者を、スクリーニング時のHIV-1 RNA量(≤100,000copies/mL vs >100,000copies/mL)及び治験担当医師が選択したNRTIで層別し、ピフェルトロ®併用群又はDRV/r(800mg/100mg)併用群に無作為に割付け、治験担当医師が選択したテノホビル ジソプロキシルフマル酸塩300mg/エムトリシタビン200mg(TDF/FTC)又はアバカビル 600mg/ラミブジン300mg(ABC/3TC)と併用して、96週間治療を行った。
[評価項目]
主要評価項目[検証的解析項目]:48週時におけるHIV-1 RNA量<50copies/mLの患者の割合
副次評価項目:96週時におけるHIV-1 RNA量<50copies/mLの患者の割合
48週時及び96週時におけるHIV-1 RNA量<40copies/mLの患者の割合
48週時及び96週時におけるCD4陽性リンパ球数のベースラインからの変化量 等
探索的評価項目:HIV-1 RNA量<200copies/mLの患者の割合、抗ウイルス薬に対する耐性変異の発現率 等
安全性評価項目:有害事象/副作用、48週時及び96週時における空腹時脂質(LDLコレステロール、Non-HDLコレステロール、HDL コレステロール、コレステロール及びトリグリセリド)のベースラインからの変化量 等
[解析計画]
有効率の群間差の95%信頼区間(CI)は、各層で投与群あたりの症例数の調和平均により重み付けした差を用いた層補正Mantel-Haenszel法により算出した。群間差(ピフェルトロ®併用群-DRV/r併用群)の95%CIの下限値が-10%を上回る場合に、DRV/r併用群に対するピフェルトロ®併用群の非劣性が検証されるとした。
主要評価項目及び96週時のHIV-1 RNA量<50copies/mLの患者の割合(副次評価項目)について、ベースライン時のHIV-1 RNA量別、ベースライン時のCD4陽性リンパ球数別及び併用するNRTIの種類についてサブグループ解析を実施した。
有効性
■抗ウイルス効果
主要評価項目である48週時におけるHIV-1 RNA量<50copies/mLの患者の割合が、ピフェルトロ®併用群83.8%、DRV/r併用群79.9%であり、群間差3.9%(95%CI:-1.6, 9.4、Mantel-Haenszel法)の95%CIの下限値が-10%を上回ったため、ピフェルトロ®併用群のDRV/r併用群に対する非劣性が検証されました。
HIV-1 RNA量<50copies/mLの患者推移a(主要評価項目[検証的解析結果]:48週時)1)2)
![HIV-1 RNA量<50copies/mLの患者推移a(主要評価項目[検証的解析結果]:48週時)](https://www.msdconnect.jp/wp-content/uploads/sites/5/2026/04/pifeltro_drive-forward_fig02.png?w=1024)
a:FDA Snapshot法:理由を問わず、試験の中止を含めて全てのデータ欠損を治療失敗として扱った。
b:背景治療としてTDF/FTC又はABC/3TCを投与
c:群間差の95%CIは、各層で投与群あたりの症例数の調和平均により重み付けした差を用いた層補正Mantel-Haenszel法により算出した。群間差(ピフェルトロ®併用群-DRV/r併用群)の95%CIの下限値が-10%を上回る場合に、DRV/r併用群に対するピフェルトロ®併用群の非劣性が検証されるとした。
ピフェルトロ®併用群は、ベースライン時のHIV-1 RNA量にかかわらず、抗ウイルス効果を示しました。
48週時におけるHIV-1 RNA量<50copies/mLの患者の割合a(主要評価項目のサブグループ解析)1)

a:Observed Failure法:効果不十分のために試験薬投与を早期に中止し、欠測値(投与期間中に断続的に生じる欠測値を除く)のある症例を治療失敗例として扱った。
b:背景治療としてTDF/FTC又はABC/3TCを投与
n:各カテゴリーに該当した患者数
■抗ウイルス効果及び免疫学的効果
ピフェルトロ®併用群の48週時及び96週時におけるウイルス学的有効性及び免疫学的有効性は、以下のとおりでした。
48週時及び96週時における投与群別のウイルス学的有効性及び免疫学的有効性2)(副次評価項目、探索的評価項目)
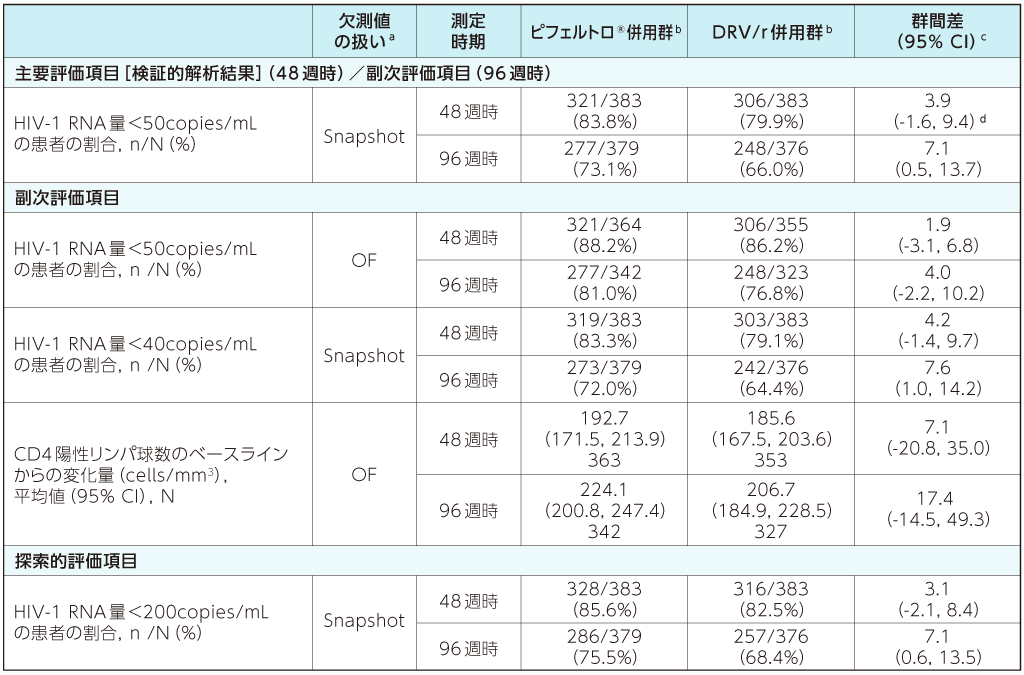
a:Snapshot:FDA Snapshot法:理由を問わず、試験の中止を含めて全てのデータ欠損を治療失敗として扱った。
OF:Observed Failure法:効果不十分のために試験薬投与を早期に中止し、欠測値(投与期間中に断続的に生じる欠測値を除く)のある症例を治療失敗例として扱った。
b:背景治療としてTDF/FTC又はABC/3TCを投与
c:群間差の95% CIは各層で投与群当たりの症例数の調和平均により重み付けした差を用いた層補正Mantel-Haenszel法により算出した。CD4陽性リンパ球数の平均変化量の差の95%CIは、t分布に基づいて求めた。
d:群間差(ピフェルトロ®併用群-DRV/r併用群)の95%CIの下限値が-10%を上回る場合に、DRV/r併用群に対するピフェルトロ®併用群の非劣性が検証されるとした。
安全性
■ 副作用
96週までの副作用発現率は、ピフェルトロ®併用群及びDRV/r併用群のいずれも32.1%(123/383例)でした。
ピフェルトロ®併用群の主な副作用は、悪心27例(7.0%)、頭痛23例(6.0%)及び下痢22例(5.7%)でした。
DRV/r併用群の主な副作用は、下痢50例(13.1%)、悪心31例(8.1%)及び頭痛10例(2.6%)でした。
試験薬と関連のある死亡は、両群ともに認められませんでした。
重篤な副作用は、ピフェルトロ®併用群の1例で悪心及び嘔吐が各1件、DRV/r併用群で末梢性浮腫1例でした。
試験薬の投与中止に至った副作用は、ピフェルトロ®併用群5例で悪心3件、腹痛2件、紅斑性皮疹、嘔吐及び斑状皮疹が各1件、DRV/r併用群8例でALT増加及びAST増加が各2件、末梢性浮腫、血中クレアチンホスホキナーゼ増加、斑状丘疹状皮疹、下痢、上腹部痛、裂孔ヘルニア、発熱、腹痛、鼓腸及び悪心が各1件でした。
■〔参考情報〕脂質プロファイルへの影響
48週時におけるLDLコレステロール及びNon-HDLコレステロールのベースラインからの変化量は、ピフェルトロ®併用群で-4.5及び-5.3mg/dL、DRV/r併用群でそれぞれ9.9及び13.8mg/dLでした。
48週時における空腹時脂質のベースラインからの変化量(安全性評価項目)2)
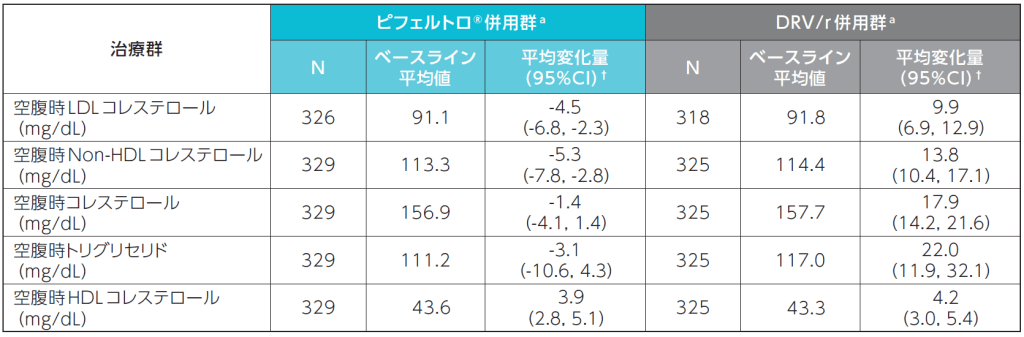
a:背景治療としてTDF/FTC又はABC/3TCを投与
欠測値は、Last Observation Carried Forward(LOCF)法を用いて補完した。
†:群内の95%CIはt分布に基づいた。
ベースライン後データは、試験薬の投与開始から最終投与の14日後までの測定結果を対象とした。
N:ベースライン後の検査結果が1つ以上得られた患者の数