PD-L1検査の臨床的意義
「警告・禁忌を含む注意事項等情報」等はこちらをご参照ください。
PD-L1検査の臨床的意義
はじめに
監修:
横浜市立大学大学院
医学研究科・医学部 分子病理学
主任教授
藤井 誠志 先生
分子標的治療薬や免疫チェックポイント阻害薬の登場、またがん遺伝子パネル検査の保険収載によりゲノム医療が行われている中、治療の適否や効果予測に関わる病理診断の重要性はますます高まっています。
そのような状況下で、キイトルーダ®は、2019年12月に「再発又は遠隔転移を有する頭頸部癌」に対する効能又は効果が承認され、2026年2月に「局所進行頭頸部癌における術前・術後補助療法」に対する効能又は効果が承認されました。キイトルーダ®はT細胞機能を負に制御するPD-L1及びPD-L2のPD-1への結合を阻害する抗体であり、PD-L1を発現する腫瘍細胞や炎症細胞が多い症例に抗腫瘍作用が期待されます。頭頸部癌症例への適応は、「コンプリメンタリー診断薬※」(PD-L1 IHC 22C3 pharmDx「ダコ」[Autostainer Link 48用])を用いた免疫組織化学的染色標本のCombined Positive Score(CPS)によって判定されます。
CPSは、腫瘍細胞に加えて、腫瘍浸潤免疫細胞(リンパ球、マクロファージ)も評価対象として陽性細胞率を算出するスコアです。本邦では、2019年に頭頸部癌の治療方針を選択するために導入され、現在では食道扁平上皮癌(2次治療以降)、進行又は再発の子宮頸癌、手術不能又は再発のトリプルネガティブ乳癌、胃癌の治療方針の選択にも使用されています。非小細胞肺癌において使用されている、腫瘍細胞のみを評価するTumor Proportion Score(TPS)とは判定方法が異なることに注意が必要です。
2019年12月の効能又は効果の承認根拠となった国際共同第Ⅲ相試験(KEYNOTE-048試験)1,2)では、再発又は遠隔転移を有する頭頸部扁平上皮癌患者において、キイトルーダ®併用群[キイトルーダ® 、プラチナ製剤及び5-FU併用療法]が、対照(EXTREMEレジメン)群に対して、有効性を示す成績が得られたことから、キイトルーダ®併用・単独において、CPSの多寡に関わらず使用可能となりました。
また、2026年2月の効能又は効果の承認根拠となった国際共同第Ⅲ相試験(KEYNOTE-689試験)3,4)では、Ⅲ又はⅣA期の局所進行頭頸部扁平上皮癌患者において、キイトルーダ®群[キイトルーダ®による術前補助療法を実施後に手術を行い、その後キイトルーダ® +放射線療法(RT)±シスプラチンの併用療法、続いてキイトルーダ®単独療法による術後補助療法]が、対照群[術前補助療法を実施せず、手術を行い、その後RT±シスプラチンによる術後補助療法]に対して、有効性を示す成績が得られたことから、キイトルーダ®による術前・術後補助療法が、CPSの多寡に関わらず使用可能となりました。
キイトルーダ®適応決定のためのPD-L1検査(病理医の解釈に基づく、医療行為による判定であり、分子病理診断になります)において、CPSについて十分にご理解いただくことは非常に重要であると考え、本コンテンツではCPSの計算方法や評価対象細胞の詳細についてページを割いて説明させていただいています。それと同時に、検体の取り扱い(固定・包埋・薄切・染色など)についても精度管理が求められることを忘れてはなりません。本コンテンツが、多くの施設におけるPD-L1検査(PD-L1分子病理診断)の標準化につながり、キイトルーダ®が頭頸部癌の治療に寄与することを希望します。
IHC:Immunohistochemistry(免疫組織化学的染色)
※ コンパニオン診断薬は、特定の医薬品の有効性や安全性が期待される患者を特定するために使用される体外診断用医薬品又は医療機器のうち、当該医薬品の使用にあたり不可欠なものです。
一方、コンプリメンタリー診断薬は、医薬品の有効性や安全性に対して参考になりますが、必須ではありません。
1)承認時評価資料:国際共同第Ⅲ相試験(KEYNOTE-048試験)
2)Burtness B, et al. Lancet 2019; 394: 1915-1928
本試験はMSD社の資金提供により行われた。Barbara BurtnessはMSD社より謝礼や旅費などを受領している。その他の著者にMSD社より謝礼などを受領している者が含まれる。
3)承認時評価資料:国際共同第Ⅲ相試験(KEYNOTE-689試験)
4)Uppaluri R, et al. N Engl J Med. 2025;393:37-50
本試験はMSD社の資金提供により行われた。著者のうち、Burak Gumuscu、Cole Manschot、Kimberly Thomasは同社の社員である。その他の著者にMSD社のコンサルタントや、講演料等を受領した者が含まれる。
5. 効能又は効果に関連する注意(抜粋)
〈再発又は遠隔転移を有する頭頸部癌〉
5.13 本剤単独投与の延命効果は、PD-L1発現率(CPS)により異なる傾向が示唆されている。CPSについて、「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.22参照]
5.14「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.22参照]
〈局所進行頭頸部癌における術前・術後補助療法〉
5.15 本剤の有効性は、PD-L1発現率(CPS)により異なる傾向が示唆されている。CPSについて、「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.23参照]
5.16 臨床試験に組み入れられた患者の病期及び病理組織型等について、「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.23参照]
頭頸部癌に関する「効能又は効果」、「用法及び用量」
効能又は効果(抜粋)
再発又は遠隔転移を有する頭頸部癌
局所進行頭頸部癌における術前・術後補助療法
効能又は効果に関連する注意(抜粋)
<再発又は遠隔転移を有する頭頸部癌>
5.13 本剤単独投与の延命効果は、PD-L1発現率(CPS)により異なる傾向が示唆されている。CPSについて、「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.22参照]
5.14「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.22参照]
〈局所進行頭頸部癌における術前・術後補助療法〉
5.15 本剤の有効性は、PD-L1発現率(CPS)により異なる傾向が示唆されている。CPSについて、「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.23参照]
5.16 臨床試験に組み入れられた患者の病期及び病理組織型等について、「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、適応患者の選択を行うこと。[17.1.23参照]
用法及び用量(抜粋)
〈再発又は遠隔転移を有する頭頸部癌〉
通常、成人には、ペムブロリズマブ(遺伝子組換え)として、1回200mgを3週間間隔又は1回400mgを6週間間隔で30分間かけて点滴静注する。
〈局所進行頭頸部癌における術前・術後補助療法〉
術前補助療法では、通常、成人には、ペムブロリズマブ(遺伝子組換え)として、1回200mgを3週間間隔又は1回400mgを6週間間隔で30分間かけて点滴静注する。その後、術後補助療法では、放射線療法又はシスプラチンを用いた化学放射線療法との併用において、ペムブロリズマブ(遺伝子組換え)として、1回200mgを3週間間隔又は1回400mgを6週間間隔で30分間かけて点滴静注する。投与回数は、3週間間隔投与の場合、術前補助療法は2回まで、術後補助療法は15回まで、6週間間隔投与の場合、術前補助療法は1回まで、術後補助療法は8回までとする。
用法及び用量に関連する注意(抜粋)
〈再発又は遠隔転移を有する頭頸部癌〉
7.5 本剤の用法及び用量は「17. 臨床成績」の項の内容を熟知し、本剤の有効性及び安全性を十分に理解した上で、選択すること。また、本剤を他の抗悪性腫瘍剤と併用する場合、併用する他の抗悪性腫瘍剤は「17. 臨床成績」の項の内容を熟知し、国内外の最新のガイドライン等を参考にした上で、選択すること。[17.1.22参照]
〈局所進行頭頸部癌における術前・術後補助療法〉
7.6 本剤と併用する放射線療法又は化学放射線療法は、「17. 臨床成績」の項の内容を熟知し、国内外の最新のガイドライン等を参考にした上で、選択すること。 [17.1.23参照]
PD-L1検査の臨床的意義
-
効果予測因子になる
PD-L1発現がキイトルーダ®の効果予測因子になり得る1-6)。 -
治療選択に役立つ
PD-L1発現(CPS:Combined Positive Score)を確認することにより、治療選択の指標となり、キイトルーダ®の適正使用に役立つ。
PD-L1 IHC 22C3 pharmDx「ダコ」(ASL48用)によるPD-L1検査のタイミング7)
局所進行頭頸部癌における術前・術後補助療法
PD-L1検査は、「局所進行頭頸部癌における術前・術後補助療法」の術前治療開始前に実施が考慮されます。
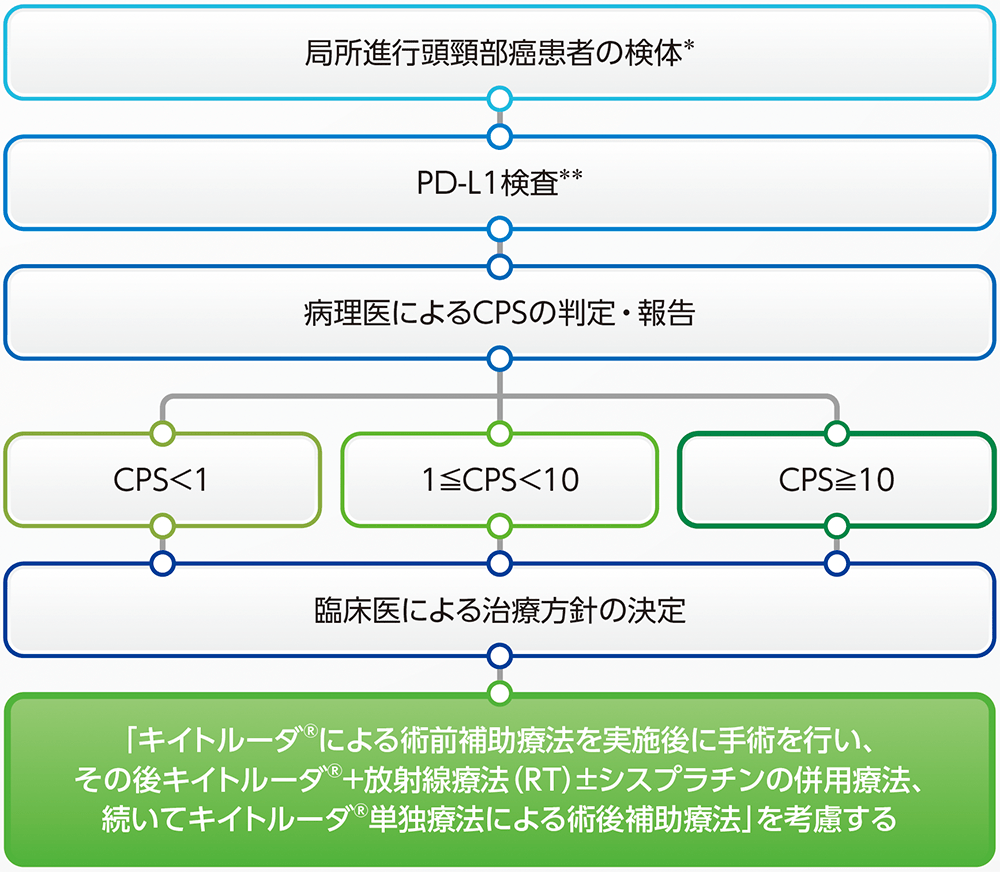
*KEYNOTE-689試験ではPD-L1検査を行うための組織は穿刺吸引(FNA)は不可
**PD-L1 IHC 22C3 pharmDx「ダコ」(ASL48用)によるPD-L1検査
再発又は遠隔転移を有する頭頸部癌
PD-L1検査は、「再発又は遠隔転移を有する頭頸部癌」の1次治療開始前に実施が考慮されます。

*PD-L1 IHC 22C3 pharmDx「ダコ」(ASL48用)によるPD-L1検査
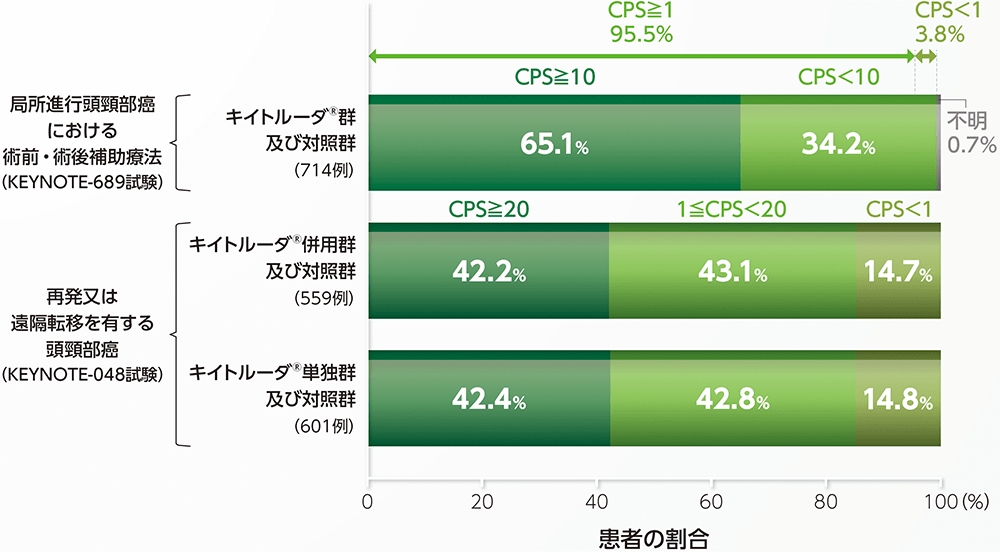
キイトルーダ®国際共同第Ⅲ相試験(KEYNOTE-689試験及びKEYNOTE-048試験)におけるPD-L1の発現状況(CPSの分布)1,5)
頭頸部癌におけるPD-L1検査(CPS)のアルゴリズム
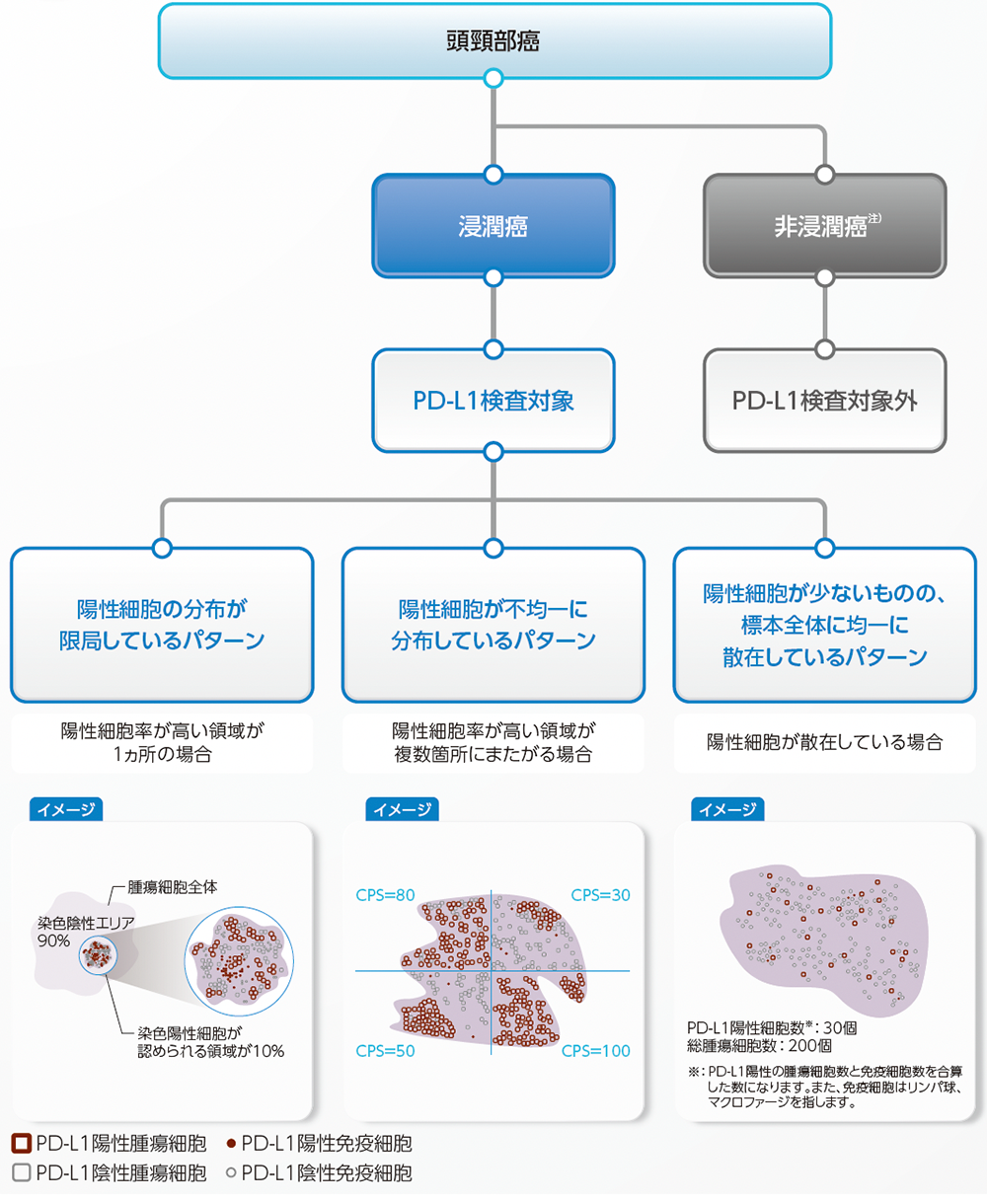
※:対象患者は「頭頸部癌」ですが、生検試料として非浸潤癌(上皮内癌)が提出された場合、PD-L1検査にはその試料を使うことはできません。
CPS(Combined Positive Score)の算出手順
CPSの算出手順7)
CPSの算出には、以下に示す計算式を用います。
腫瘍細胞は浸潤腫瘍細胞のみが対象になります。
計算式8)
※:CPSの評価において、分子あるいは分母に組み入れる細胞あるいは除外する細胞の種類については、下記の「頭頸部癌におけるCPS評価においてPD-L1陽性細胞として加算すべき細胞」をご参照ください。

● 参考)TPS(Tumor Proportion Score)の計算式

Ⅳ期非小細胞肺癌におけるPD-L1検査では、TPSが指標として用いられており、腫瘍細胞のみが評価対象細胞となっています。
頭頸部癌におけるCPS評価においてPD-L1陽性細胞として加算すべき細胞
CPS計算式における分子および分母の組み入れ/除外基準7)
CPSの評価において、計算式の分子あるいは分母に組み入れる細胞あるいは除外する細胞の種類は以下の表に示す通りです。
* MICでは、細胞質に対する細胞核の比率が高いため、多くの場合細胞膜染色と細胞質染色とは判別不能です。
このため、 MICの細胞膜または細胞質染色はスコアリングに含まれます。
† 隣接するMICは腫瘍と同じ20倍視野内にあると定義されます。しかし、腫瘍に対する反応に直接関連しないMICは除外されます。
‡ マクロファージと組織球は同じ細胞と判断します。
● 参考)染色強度1+(弱陽性)以上の染色像7)
■頭頸部癌:国際共同臨床試験成績:国際共同第Ⅲ相試験 <KEYNOTE-048試験>の概要
■頭頸部癌:国際共同臨床試験成績:国際共同第Ⅲ相試験 <KEYNOTE-689試験>の概要
引用文献
1)承認時評価資料:国際共同第Ⅲ相試験(KEYNOTE-048試験)
2)Burtness B et al. Lancet 2019; 394: 1915-1928
(本試験はMSD社の資金提供により行われた。Barbara BurtnessはMSD社より謝礼や旅費などを受領している。その他の著者にMSD社より謝礼などを受領している者が含まれる)
3)Chow LQM, et al. J Clin Oncol. 2016; 34: 3838-3845
4)Bauml J, et al. J Clin Oncol. 2017; 35: 1542-1549
5)承認時評価資料:国際共同第Ⅲ相試験(KEYNOTE-689試験)
6)Uppaluri R, et al. N Engl J Med. 2025; 393: 37-50
(本試験はMSD社の資金提供により行われた。著者のうち、Burak Gumuscu、Cole Manschot、Kimberly Thomasは同社の社員である。その他の著者にMSD社のコンサルタントや、講演料等を受領した者が含まれる)
7)PD-L1 IHC 22C3 pharmDx「ダコ」頭頸部癌染色結果判定マニュアル
8)PD-L1 IHC 22C3 pharmDx「ダコ」(Code No. SK006)電子添文