国際共同第Ⅲ相試験:KEYNOTE-826試験(日本人集団)
子宮頸癌:国際共同臨床試験成績
国際共同第Ⅲ相試験<KEYNOTE-826試験>(日本人集団)
承認時評価資料:国際共同第Ⅲ相試験(KEYNOTE-826試験)
日本人集団における患者背景(ITT集団)
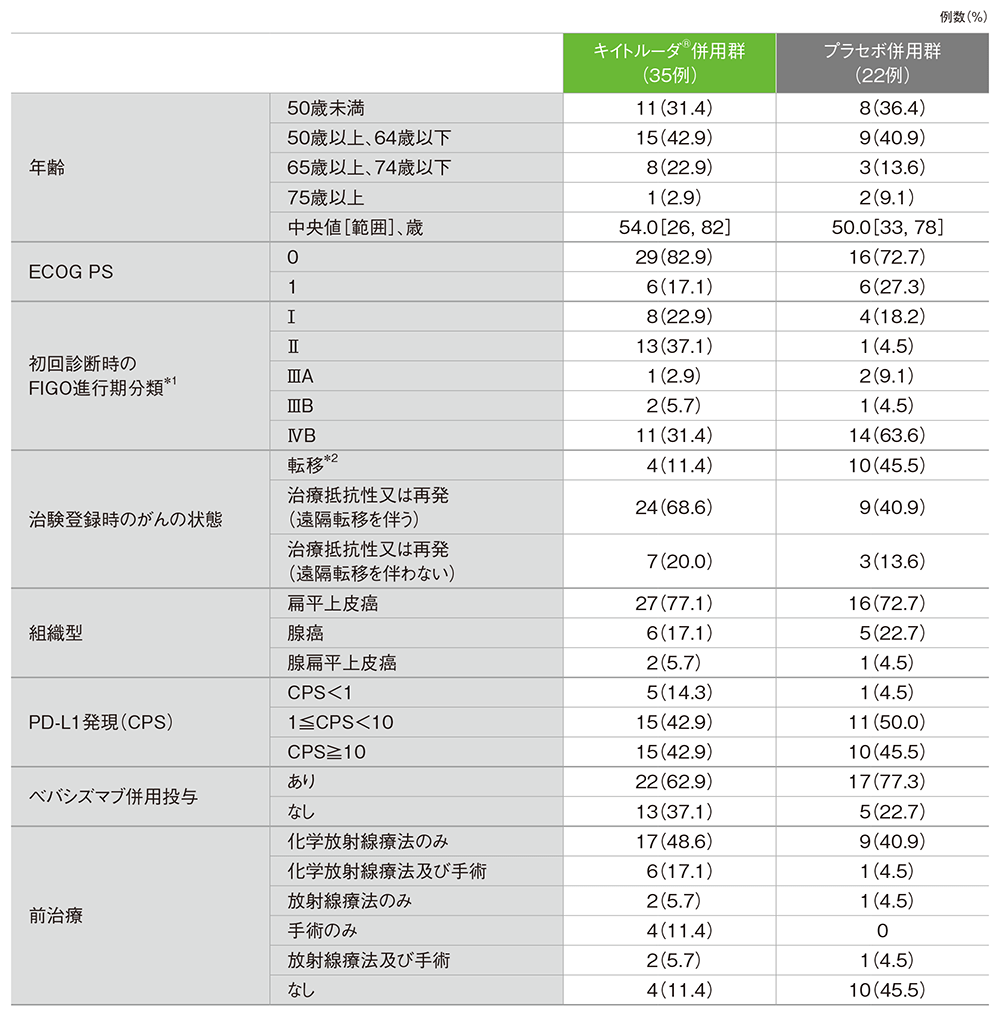
*1 FIGO 2009/NCCN 2017基準によって定義された
*2 子宮頸癌に対するいかなる治療も受けていない、遠隔転移を有する(ステージⅣB期)患者。傍大動脈リンパ節転移のある患者を含む(注)
注:FIGO 2009分類では傍大動脈リンパ節転移はⅣB期に含まれるが、FIGO 2018分類では傍大動脈リンパ節転移はⅣB期に含まれない
本治験では、初回診断時の傍大動脈リンパ節転移を遠隔転移として扱う
サブグループ解析:日本人集団における全生存期間(OS)
■日本人集団における全生存期間: OS
- OS中央値はキイトルーダ®併用群で未到達(95%CI: NE, NE)、プラセボ併用群で25.0ヵ月(95%CI: 15.7, NE)でした。
OSのKaplan-Meier曲線(ITT集団)
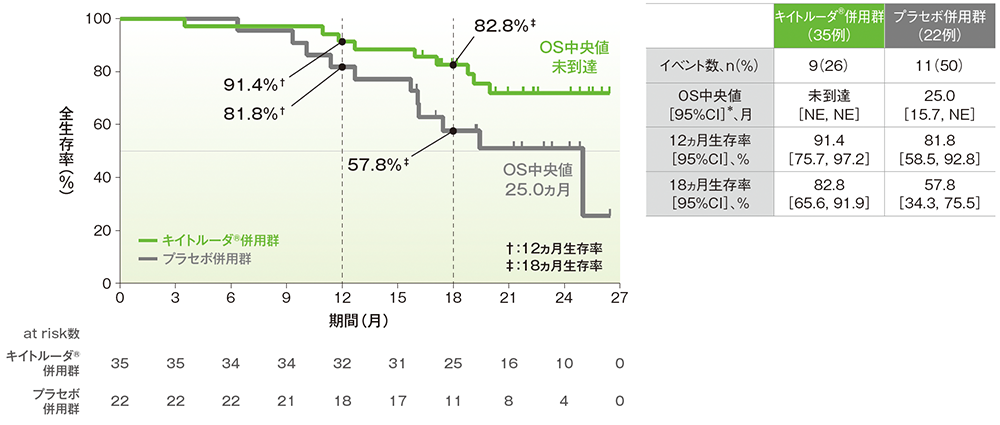
* 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:キイトルーダ®併用群 21.5ヵ月、プラセボ併用群 18.4ヵ月、データカットオフ日:2021年5月3日)
NE:Not Estimated
■PD-L1発現陽性(CPS≧1)患者における全生存期間:OS(日本人集団)
- OS中央値はキイトルーダ®併用群で未到達(95%CI: NE, NE)、プラセボ併用群で25.0ヵ月(95%CI: 15.7, NE)でした。
OSのKaplan-Meier曲線(ITT集団)
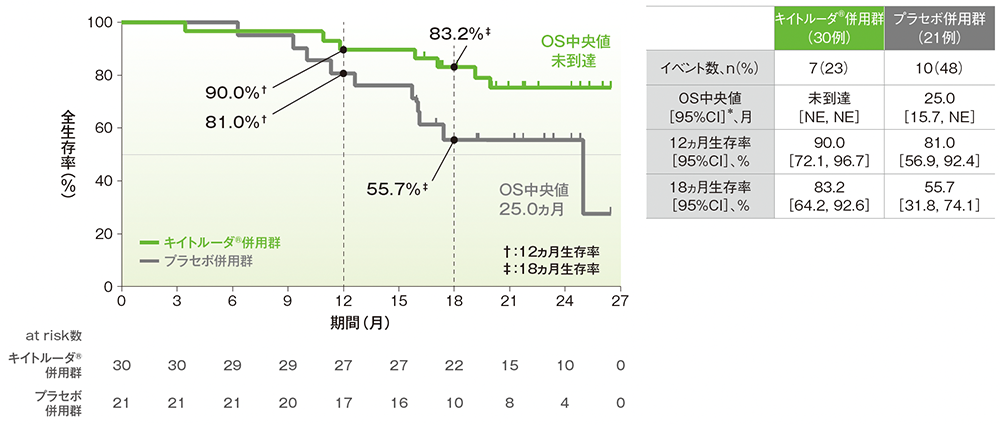
* 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:キイトルーダ®併用群 21.5ヵ月、プラセボ併用群 18.4ヵ月、データカットオフ日:2021年5月3日)
NE:Not Estimated
■PD-L1発現陽性(CPS≧10)患者における全生存期間:OS(日本人集団)
- OS中央値はキイトルーダ®併用群で未到達(95%CI: 17.1, NE)、プラセボ併用群で21.2ヵ月(95%CI: 6.3, NE)でした。
OSのKaplan-Meier曲線(ITT集団)
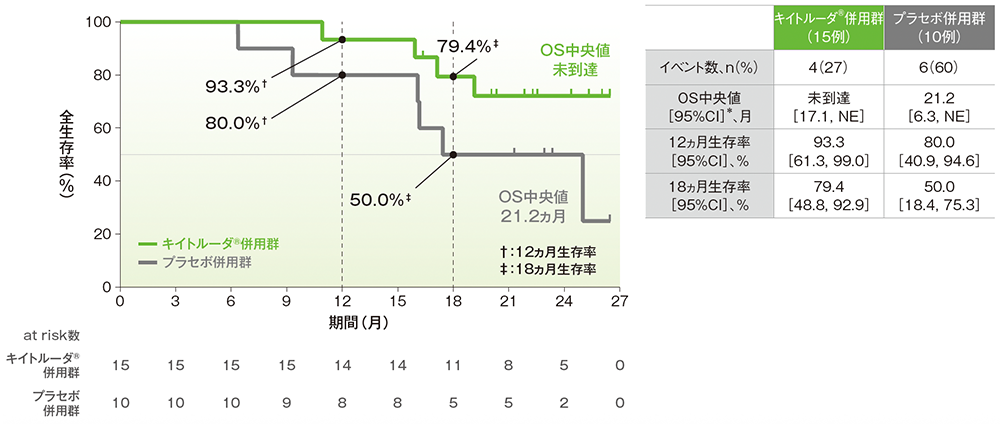
* 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:キイトルーダ®併用群 21.5ヵ月、プラセボ併用群 18.4ヵ月、データカットオフ日:2021年5月3日)
NE:Not Estimated
サブグループ解析:日本人集団における無増悪生存期間(PFS)、日本人集団における12ヵ月PFS率
■日本人集団における無増悪生存期間:PFS
■日本人集団における12ヵ月PFS率
- PFS中央値は、キイトルーダ®併用群で未到達(95%CI: 10.2, NE)、プラセボ併用群で11.5ヵ月(95%CI: 8.1, 13.6)でした。
- 12ヵ月PFS率はキイトルーダ®併用群で65.0%(95%CI: 46.6, 78.4)、プラセボ併用群で47.6%(95%CI: 25.7, 66.7)でした。
PFSのKaplan-Meier曲線(ITT集団)
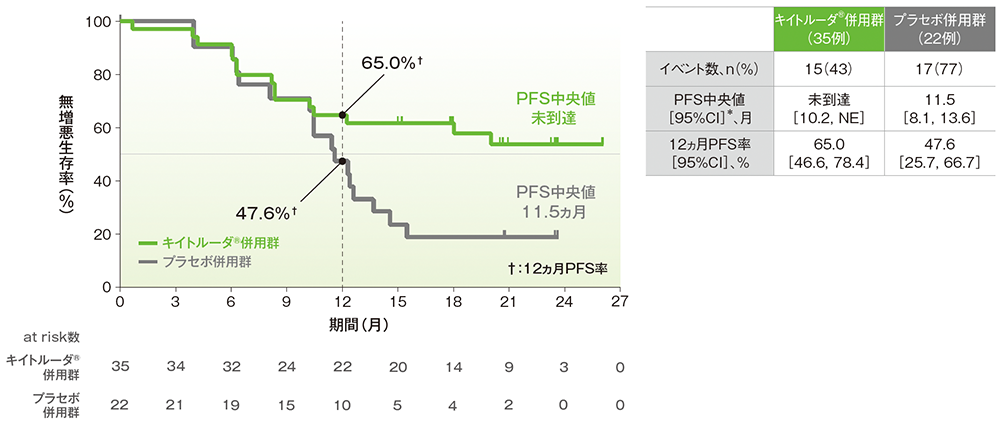
治験担当医師によるRECISTガイドライン1.1版に基づいた評価
* 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:キイトルーダ®併用群 21.5ヵ月、プラセボ併用群 18.4ヵ月、データカットオフ日:2021年5月3日)
NE:Not Estimated
■PD-L1発現陽性(CPS≧1)患者における無増悪生存期間:PFS(日本人集団)
■PD-L1発現陽性(CPS≧1)患者における12ヵ月PFS率(日本人集団)
- PFS中央値は、キイトルーダ®併用群で未到達(95%CI: 12.2, NE)、プラセボ併用群で11.9ヵ月(95%CI: 6.4, 14.5)でした。
- 12ヵ月PFS率はキイトルーダ®併用群で72.7%(95%CI: 52.7, 85.3)、プラセボ併用群で50.0%(95%CI: 27.1, 69.2)でした。
PFSのKaplan-Meier曲線(ITT集団)
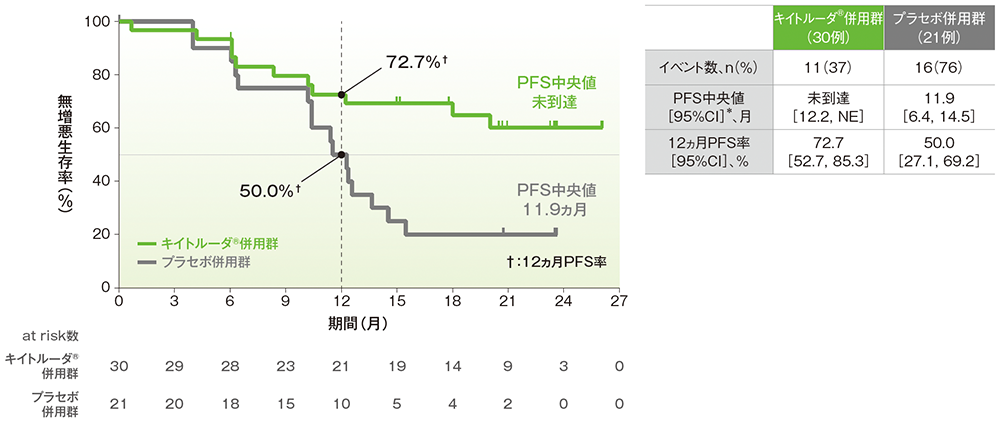
治験担当医師によるRECISTガイドライン1.1版に基づいた評価
* 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:キイトルーダ®併用群 21.5ヵ月、プラセボ併用群 18.4ヵ月、データカットオフ日:2021年5月3日)
NE:Not Estimated
■PD-L1発現陽性(CPS≧10)患者における無増悪生存期間:PFS(日本人集団)
■PD-L1発現陽性(CPS≧10)患者における12ヵ月PFS率(日本人集団)
- PFS中央値は、キイトルーダ®併用群で未到達(95%CI: 6.3, NE)、プラセボ併用群で12.3ヵ月(95%CI: 4.0, 14.5)でした。
- 12ヵ月PFS率はキイトルーダ®併用群で65.0%(95%CI: 35.1, 83.7)、プラセボ併用群で55.6%(95%CI: 20.4, 80.5)でした。
PFSのKaplan-Meier曲線(ITT集団)
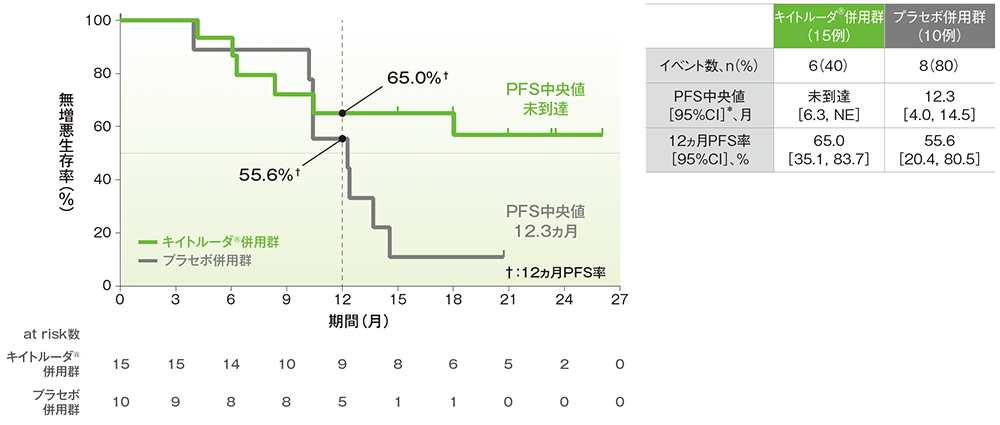
治験担当医師によるRECISTガイドライン1.1版に基づいた評価
* 打ち切りデータはproduct-limit(Kaplan-Meier)法に基づく
(追跡期間中央値:キイトルーダ®併用群 21.5ヵ月、プラセボ併用群 18.4ヵ月、データカットオフ日:2021年5月3日)
NE:Not Estimated
安全性
■日本人集団における主な副作用(いずれかの投与群で発現率5%以上)(APaT集団)
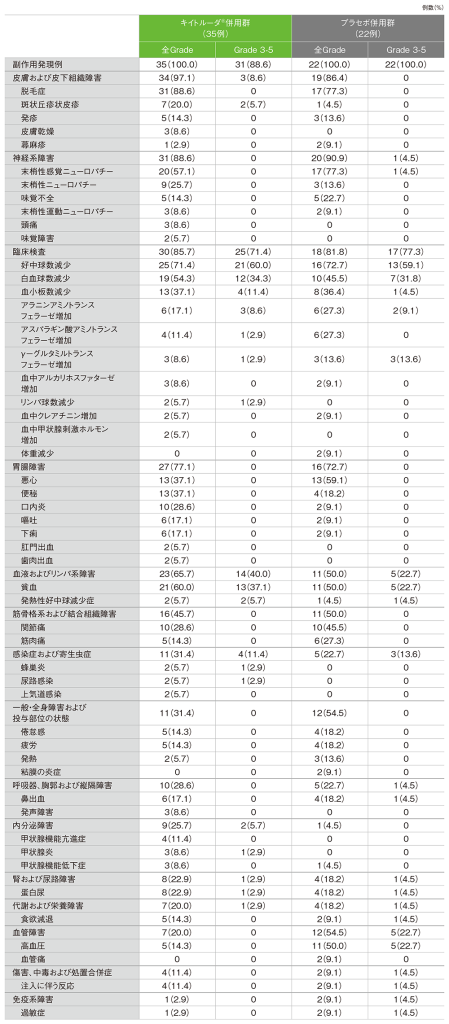
MedDRA/J v24.0、GradeはCTCAE v 4.0
(データカットオフ日:2021年5月3日)
■免疫関連など特に注目すべき有害事象(APaT集団)※
※カテゴリー別で集計
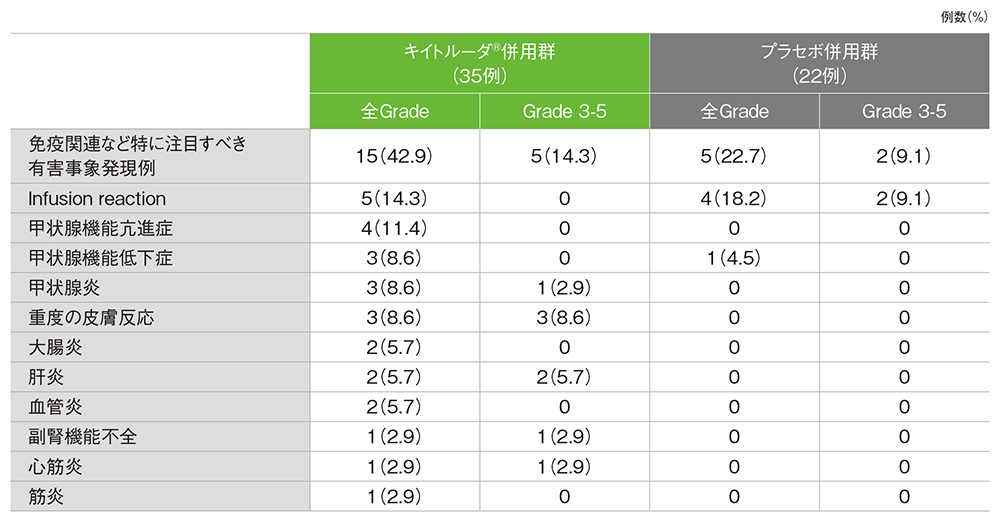
MedDRA/J v24.0、GradeはCTCAE v 4.0
(データカットオフ日:2021年5月3日)


