疾患啓発リーフ(これからの自分のために肺炎予防していますか)
肺炎予防についてお伝えいただける疾患啓発リーフです。
承認時評価資料:国際共同第Ⅲ相試験(006試験)
Scott P, et al. Clin Infect Dis . 2024: 79(6):1366-1374.
[利益相反:本研究はMSD社からの支援により実施され、著者には同社の社員および株式を保有している者が含まれている。]
各コホートに承認外の50~64歳の健康成人が含まれるが、承認時評価資料として評価されたため掲載する。
コホート1、2:無作為化、実薬対照、並行群間、多施設共同、二重盲検比較試験
コホート3:多施設共同、非盲検単群試験

PPSV23:23価肺炎球菌莢膜ポリサッカライドワクチン
PCV13:沈降13価肺炎球菌結合型ワクチン
PCV15:沈降15価肺炎球菌結合型ワクチン
PCV20:沈降20価肺炎球菌結合型ワクチン
| 目的 | 肺炎球菌ワクチン接種歴がある50歳以上の成人を対象に、キャップバックス®の安全性、忍容性および免疫原性を検討する。 |
| 対象 | 侵襲性肺炎球菌感染症の既往歴がないかつ組み入れの1年以上前に肺炎球菌ワクチン接種歴がある50歳以上の成人717例(65歳以上の日本人63例を含む) |
| 方法 | コホート1ではPPSV23の接種歴がある被験者をキャップバックス®群またはPCV15群に2:1の比で無作為に割り付け、キャップバックス®またはPCV15 0.5mLを単回筋肉内接種した。 コホート2ではPCV13の接種歴がある被験者をキャップバックス®群またはPPSV23群に2:1の比で無作為に割り付け、キャップバックス®またはPPSV23 0.5mLを単回筋肉内接種した。 コホート3 ではPCV13 + PPSV23、PCV15 + PPSV23、PCV15、PCV20 またはPPSV23 + PCV13 の接種歴がある被験者にキャップバックス®0.5mL を単回筋肉内接種した。 免疫原性は、ワクチン接種後30日目に検討した。安全性は、ワクチン接種後1~5日目までの事前に規定した有害事象、試験期間中の重篤な副反応を検討した。 |
| 評価項目 | 【免疫原性】 主要評価項目: キャップバックス®、PCV15またはPPSV23接種後30日目におけるキャップバックス® が含有する全血清型(3、6A、7F、8、9N、10A、11A、12F、15A、15C、16F、17F、19A、20A、22F、23A、23B、24F、31、33F、35B)に対する血清型特異的OPA GMT 副次評価項目: キャップバックス®、PCV15またはPPSV23接種前から接種後30日目までのキャップバックス® が含有する全血清型(3、6A、7F、8、9N、10A、11A、12F、15A、15C、16F、17F、19A、20A、22F、23A、23B、24F、31、33F、35B)に対する血清型特異的OPA応答の上昇倍率が4倍以上であった被験者割合 【安全性】 主要評価項目: キャップバックス®、PCV15またはPPSV23 接種後1~5日目までの事前に規定した注射部位の有害事象(疼痛、腫脹、紅斑)、接種後1~5日目までの事前に規定した全身性の有害事象(疲労、頭痛、筋肉痛、発熱)、試験期間中の重篤な副反応 |
| 解析計画 | 【免疫原性】 免疫原性の解析には治験実施計画書を逸脱していない全ての被験者(PP 集団)を用いた。血清型特異的OPA GMTは記述統計量および各接種群内での95%CIを含めて評価した。 主要評価項目: キャップバックス® が含有する全血清型(3、6A、7F、8、9N、10A、11A、12F、15A、15C、16F、17F、19A、20A、22F、23A、23B、24F、31、33F、35B)の血清型特異的OPA GMTを求め、評価したa。 副次評価項目: キャップバックス® が含有する全血清型(3、6A、7F、8、9N、10A、11A、12F、15A、15C、16F、17F、19A、20A、22F、23A、23B、24F、31、33F、35B)のOPA応答の上昇倍率が4倍以上であった被験者の割合を求め、評価したb。 a 連続量の評価項目の点推定値は自然対数変換した平均値を逆変換することにより算出し、接種群ごとのCI は自然対数変換した平均値のt分布に基づくCI を逆変換し算出。 b 離散型の評価項目のCIはClopperとPearson による正確法に基づき算出。 【安全性】 安全性の解析には無作為化され、ワクチンを接種した全ての被験者(APaT 集団)を用いた。安全性の評価は、 記述統計量により各コホートの各接種群内で要約した。 |
4. 効能又は効果
高齢者又は肺炎球菌による疾患に罹患するリスクが高いと考えられる成人における肺炎球菌による感染症の予防
5. 効能又は効果に関連する注意(抜粋)
5.3 肺炎球菌による疾患に罹患するリスクが高いと考えられる成人とは、以下のような状態の者を指す。
・ 慢性的な心疾患、肺疾患、肝疾患又は腎疾患
・ 糖尿病
・ 基礎疾患若しくは治療により免疫不全状態である又はその状態が疑われる者
・ 先天的又は後天的無脾症
・ 鎌状赤血球症又はその他の異常ヘモグロビン症
・ 人工内耳の装用、慢性髄液漏等の解剖学的要因により生体防御能が低下した者
・ 上記以外で医師が本剤の接種を必要と認めた者
安全性
有害事象を1件以上発現した被験者の割合は、キャップバックス®群(APaT集団509例)で265例(52.1%)、PCV15群(APaT集団117例)で75例(64.1%)、PPSV23群(APaT集団85例)で56例(65.9%)でした。
APaT(All participants as treated)集団:無作為化され、ワクチンを接種した全ての被験者
免疫原性
コホート1
コホート2
コホート3
※1 免疫応答:ワクチン接種後 30 日目の血清型特異的 OPA GMT
※2 探索的解析結果
※3 PCV13+PPSV23、PCV15+PPSV23、PCV15、PCV20またはPPSV23+PCV13の接種歴
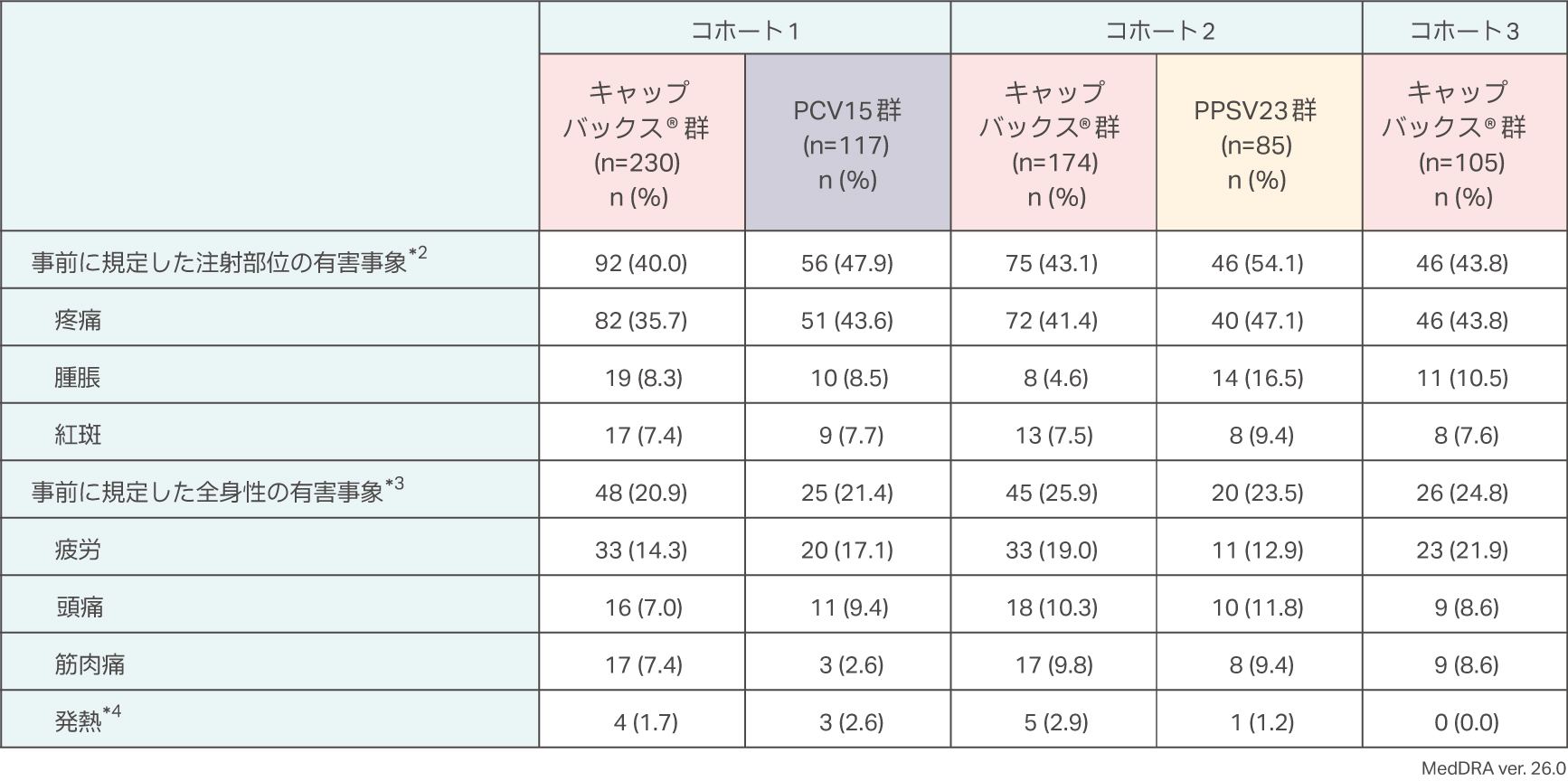
*1 APaT(All Participants as Treated)集団:ワクチンを接種した全ての被験者
*2 接種後1~5日までに疼痛、腫脹、紅斑のいずれかが1件以上発現した数
*3 接種後1~5日までに疲労、頭痛、筋肉痛、発熱のいずれかが1件以上発現した数
*4 体温は接種後1~5日目に測定され、38.0℃以上を発熱とみなした。
重篤な副反応は、コホート1のキャップバックス®群の1例(注射部位蜂巣炎)がワクチン接種後6日目に発現しましたが、回復が認められました。コホート2およびコホート3では重篤な副反応は認められませんでした。
有害事象を1件以上発現した被験者の割合は、キャップバックス®群(APaT集団509例)で265例(52.1%)、PCV15群(APaT 集団117 例)で75 例(64.1%)、PPSV23 群(APaT 集団85 例)で56 例(65.9%)であった。各コホートの主な有害事象は下記の通りでした。
コホート1:キャップバックス®群では、注射部位疼痛82例(35.7%)、疲労33例(14.3%)、注射部位腫脹20例(8.7%)、PCV15 群では、注射部位疼痛51例(43. 6%)、疲労20 例(17. 1%)、頭痛11例(9. 4%)でした。
コホート2:キャップバックス®群では、注射部位疼痛72例(41.4%)、疲労33例(19.0%)、頭痛18例(10.3%)、PPSV23群では、注射部位疼痛40例(47.1%)、注射部位腫脹14例(16.5%)、疲労12例(14.1%)でした。
コホート3:キャップバックス®群では、注射部位疼痛46例(43.8%)、疲労23例(21.9%)、注射部位腫脹11例(10.5%)で
重篤な有害事象はキャップバックス®群で6例(1.2%)に認められ、うっ血性心不全、注射部位蜂巣炎、肛門裂傷、慢性閉塞性肺疾患、胆石症、尿路感染症、各1件でした。PCV15群では4例(3.4%)に認められ、心不全、心筋虚血、大動脈腸管瘻、マロリーワイス症候群、小腸穿孔、肺炎、低血圧、各1件でした。 PPSV23群では3例(3.5%)に認められ、胆管炎、虚血性脳卒中、慢性閉塞性肺疾患、各1件でした。死亡はキャップバックス®群、PCV15群、PPSV23群の全ての群で認められませんでした。
コホート1: PPSV23接種歴あり(キャップバックス® 群 vs.PCV15群)
コホート1: キャップバックス®群は、PCV15と共通の6血清型に対して接種後30日目OPA GMTで、PCV15群と同程度の免疫応答*を、キャップバックス®固有の15血清型に対して、PCV15群より高い免疫応答を誘導しました**。
PCV15と共通する6血清型

* 免疫応答:ワクチン接種後30日目の血清型特異的OPA GMT **探索的解析結果
PP 集団
連続量の評価項目の点推定値は自然対数変換した平均値を逆変換することにより算出し、接種群ごとのCI は自然対数変換した平均値のt 分布に基づくCIを逆変換し算出した。
キャップバックス®固有の15固有血清型

* 免疫応答:ワクチン接種後30日目の血清型特異的OPA GMT **探索的解析結果
PP 集団
連続量の評価項目の点推定値は自然対数変換した平均値を逆変換することにより算出し、接種群ごとのCI は自然対数変換した平均値のt 分布に基づくCIを逆変換し算出した。
コホート2: PCV13接種歴あり(キャップバックス® 群 vs.PPSV23群)
キャップバックス®群は、PPSV23と共通の12血清型に対して接種後30日目OPA GMTで、PPSV23群と同程度の免疫応答*を、キャップバックス®固有の9血清型に対して、PPSV23群より高い免疫応答を誘導しました**。
PPSV23と共通する12血清型

* 免疫応答:ワクチン接種後30日目の血清型特異的OPA GMT **探索的解析結果
PP 集団
連続量の評価項目の点推定値は自然対数変換した平均値を逆変換することにより算出し、接種群ごとのCI は自然対数変換した平均値のt 分布に基づくCIを逆変換し算出した。
キャップバックス®固有の9固有血清型

*免疫応答:ワクチン接種後30 日目の血清型特異的OPA GMT **探索的解析結果
PP 集団
連続量の評価項目の点推定値は自然対数変換した平均値を逆変換することにより算出し、接種群ごとのCI は自然対数変換した平均値のt 分布に基づくCIを逆変換し算出した。
コホート3: その他接種歴あり(キャップバックス®群)
キャップバックス®群は含有する全ての血清型において、接種後30日目OPA GMTで、免疫応答*を誘導しました。

* 免疫応答:ワクチン接種後30 日目の血清型特異的OPA GMT
PP集団
連続量の評価項目の点推定値は自然対数変換した平均値を逆変換することにより算出し、CIは自然対数変換した平均値のt分布に基づくCIを逆変換し算出した。

肺炎予防についてお伝えいただける疾患啓発リーフです。

キャップバックス®の接種を希望される方に、接種の対象者と接種間隔、また肺炎球菌性肺炎にかかるリスクが高い方を説明する際にご利用いただける資材です。


肺炎予防についてお伝えいただける疾患啓発リーフです。


このサイトでは、医療用医薬品を適正にご使用いただくため、医師、歯科医師及び薬剤師などの医療関係者の方を対象に、主としてMSD株式会社の医療用医薬品に関する情報を提供しています。
下記の「はい」をクリックした場合、「MSD Connect ご利用規約」及び「ウェブサイトのご利用条件」を理解したうえで、内容に同意したものとみなします。
2024年11月にご利用規約を改訂致しました。上記リンクよりご確認ください。
あなたは医療関係者ですか?