国際共同第Ⅲ相試験(051試験)
国際共同第Ⅲ相試験(051試験)
ARTによりウイルス学的抑制が得られているHIV-1感染症患者を対象とした非盲検試験
承認時評価資料:国際共同第Ⅲ相試験(051試験)
1.試験概要
目的:抗レトロウイルス療法(ART)によりウイルス学的抑制が得られているHIV-1感染症患者を対象に、イドビンソ®配合錠に切り替えた場合の有効性及び安全性を、ベースラインARTを継続した場合と比較検討する。
試験デザイン:多施設共同、無作為化、非盲検、実薬対照第Ⅲ相、非劣性検証試験
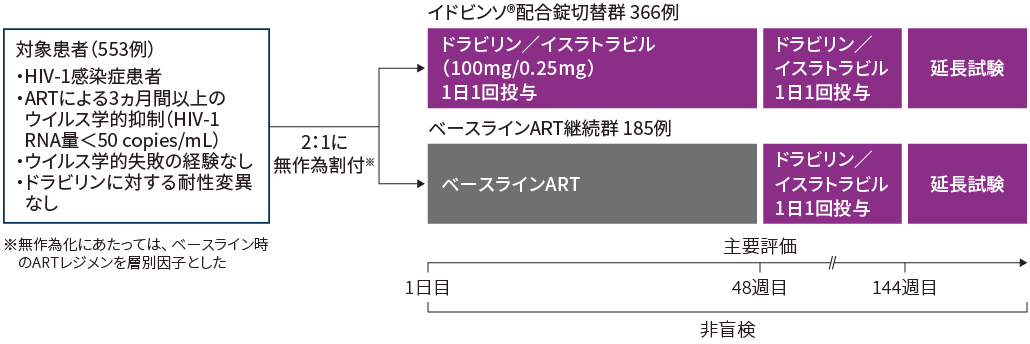
対象:2剤又は3剤の経口剤を併用したARTによりウイルス学的抑制(HIV-1 RNA量50 copies/mL未満)が3ヵ月間以上得られており、ウイルス学的失敗の経験がなく、ドラビリンに対する耐性変異が確認されていない18歳以上のHIV-1感染症患者553例※(日本人13例を含む)
※活動性HBV感染患者(HBs 抗原陽性又はHBV DNA陽性)は本試験から除外
方法:対象患者を1日目にベースラインARTからイドビンソ®配合錠(ドラビリン 100mg/イスラトラビル 0.25mg)の1日1回投与に切り替えたイドビンソ®配合錠切替群と、ベースラインARTを継続したベースラインART継続群に2:1で無作為に割り付けた。無作為化にあたっては、ベースライン時のARTレジメンで層別化した。ベースラインART継続群は48週時にイドビンソ®配合錠に切り替えた。
評価項目(有効性):
主要評価項目
HIV-1 RNA量≧50 copies/mLの患者の割合(48週時)(検証的解析項目)
副次評価項目
HIV-1 RNA量<50 copies/mLの患者の割合(48週時)
耐性変異の発現(48週時)
-ベースライン時のHIV-1プロウイルスDNAにM184I/V変異が認められた患者におけるHIV-1 RNA量<50 copies/mLの患者の割合(48週時)
CD4陽性T細胞数のベースラインからの平均変化量(48週時)等
探索的評価項目
ベースライン時の患者背景別にみたHIV-1 RNA量<50 copies/mLの患者の割合(48週時)等
評価項目(安全性):
主要評価項目
有害事象(48週時)
その他の重要な安全性評価項目
腎機能、ベースラインARTにINSTIを含む患者における空腹時脂質プロファイル(PI+INSTIレジメン及び脂質低下薬服用患者を除く)、体重のベースラインからの平均変化量(それぞれ48週時)等
解析計画:
有効性解析の主要な解析集団は、治験薬を1回以上投与され、かつべースライン時のデータを有する患者と定義するFAS集団とした。無作為化時にベースラインARTレジメンを補正した。
HIV-1 RNA量の欠測値の取扱いには、FDA Snapshot法を用いた。患者割合の群間差の95%CIは、ベースラインARTレジメンを層別因子とし、Cochran-Mantel-Haenszel(CMH)の重みを用いた層別MN法に基づき算出した。
主要評価項目の群間差(イドビンソ®配合錠切替群-ベースラインART継続群)の多重性を調整した両側95%CIの上限が4%未満の場合に、イドビンソ®配合錠切替群はベースラインART継続群に対して非劣性であるとした。
副次評価項目である耐性変異の発現は、各治療薬に対する遺伝子型又は表現型の耐性を示した薬剤耐性解析対象集団の例数を48週時点で投与群ごとに要約した。
FAS-R 集団には、ベースラインにプロウイルスDNA耐性データを有する被験者を含めた。
CD4陽性T細胞数のベースラインからの平均変化量の各群の95%CIはt分布に基づいて算出し、平均値の群間差及び95%CIは、各群のベースラインは同一で、投与後の各時点における各群の平均は異なり得ると仮定したcLDAモデルを用いて推定した。解析モデルには投与群、時点、時点と投与群の交互作用を含めた。
探索的評価項目として48週時のHIV-1 RNA量<50 copies/mLの患者の割合についてベースライン時の患者背景別(年齢、性別、地域、人種、民族、慢性C型肝炎の状態、ベースライン時のNRTI、ベースラインARTの治療期間、補正後のベースラインART)にサブグループ解析を実施した。サブグループ解析の群間差の推定値(及び層別しないMN法を用いた95%CI)についてはベースライン別の分類変数で計算し、欠測値の取扱いにはFDA Snapshot法を用いた。
安全性解析対象集団は、無作為化され、治験薬が1回以上投与された患者のAPaT集団とした。
その他の重要な安全性評価項目である48週時の腎機能、脂質、体重のベースラインからの平均変化量の95%CIはt分布に基づき算出した。
主要評価項目である48週までの中間解析結果を提示するが、本試験の主要パートは144週間であり、試験は継続中である。
2.患者背景(FAS)
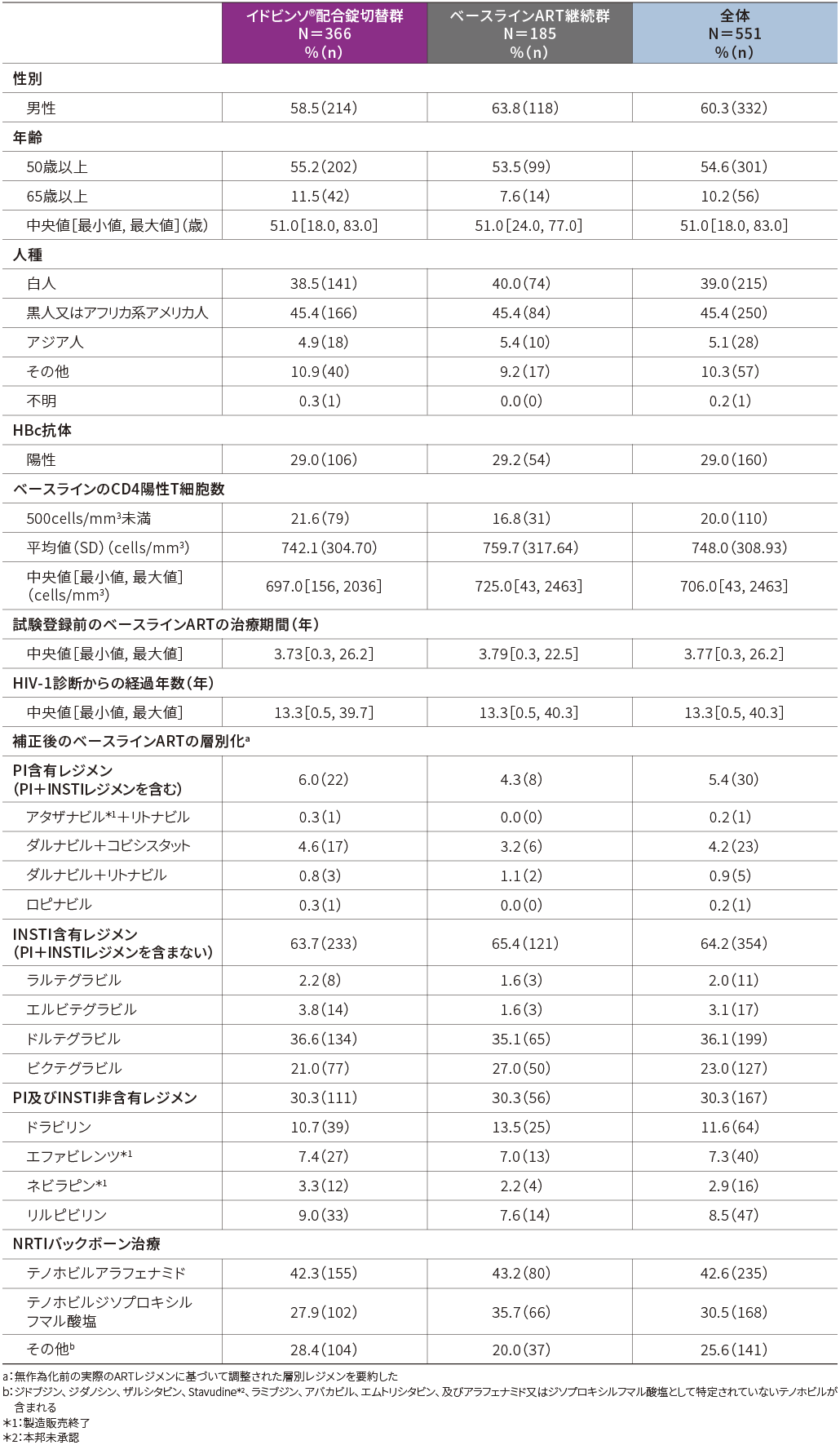
3.有効性
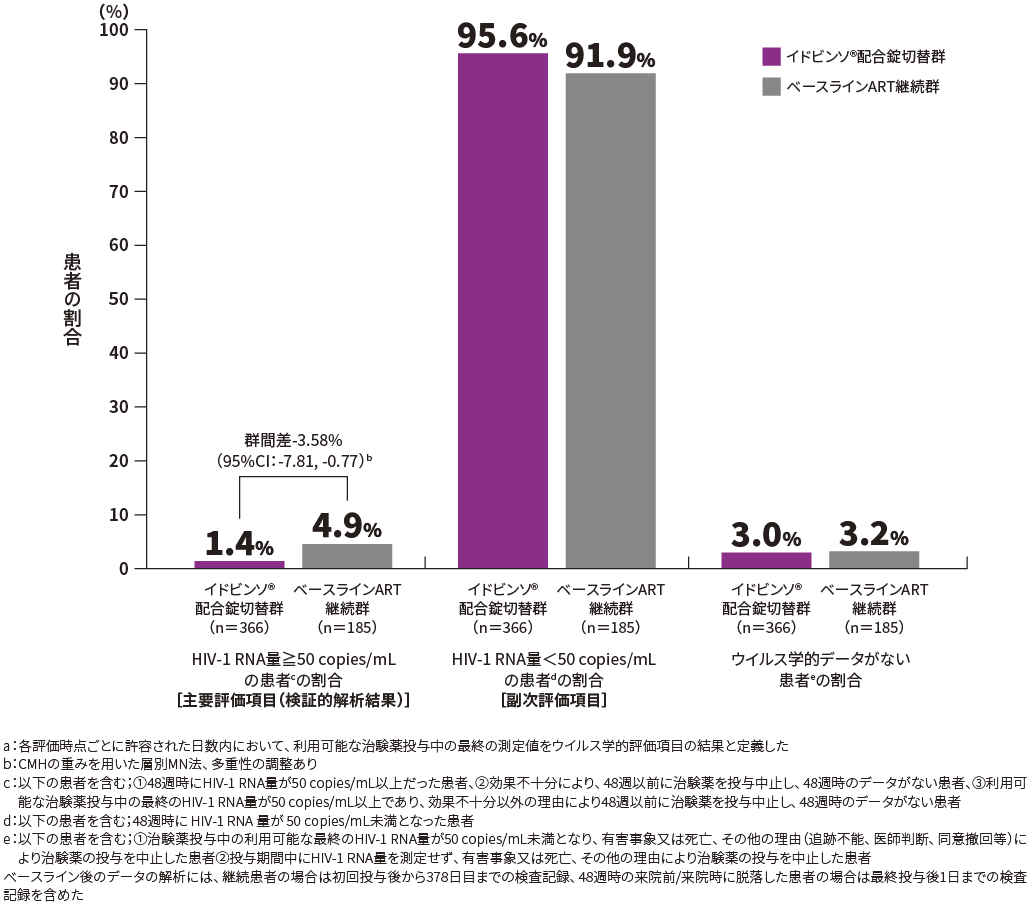
■ウイルス学的有効性(48週時・FAS)[主要評価項目(検証的解析結果)・副次的評価項目]
48週時におけるHIV-1 RNA量≧50 copies/mLの患者の割合は、イドビンソ®配合錠切替群1.4%(5/366例)、ベースラインART継続群4.9%(9/185例)、群間差-3.58%(95%CI*:-7.81,-0.77)であり、95%CIの上限が4%を下回ったため、イドビンソ®配合錠切替群のベースラインART継続群に対する非劣性が検証されました。
*:CMHの重みを用いた層別MN法、多重性の調整あり
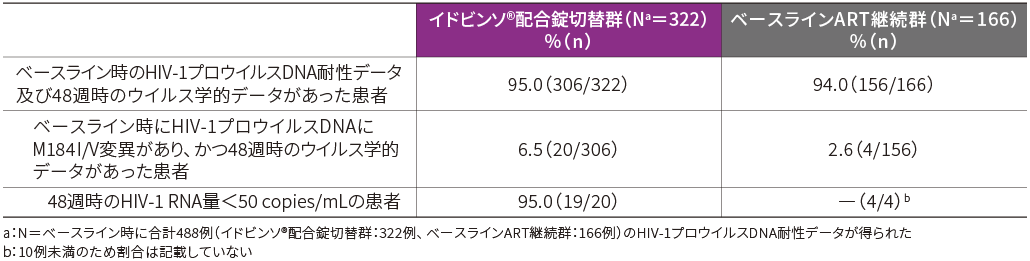
HIV-1 RNA量≧50 copies/mL、又は<50 copies/mLの患者の割合(48週時・FAS)[FDA Snapshot法a]
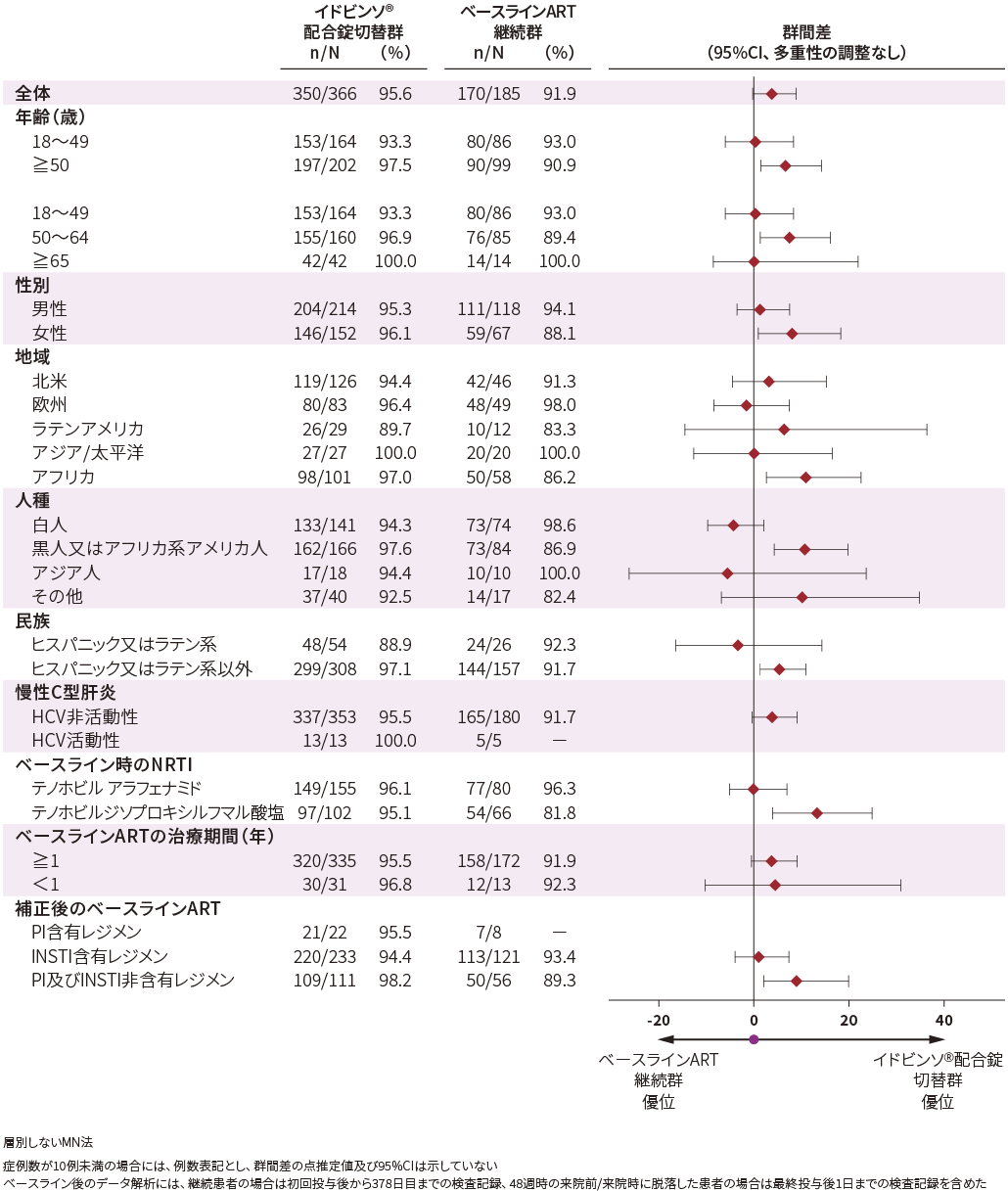
■事前規定された有効性サブグループ解析(48週時・FAS)[探索的評価項目]
ベースライン時の患者背景別にみた48週時におけるHIV-1 RNA量<50 copies/mLの患者の割合は以下の通りでした。
HIV-1 RNA量<50 copies/mLの患者の割合(48週時・FAS)[FDA Snapshot法]
■耐性変異の発現(48週時・FAS)[副次評価項目]
48週時までに、本剤に対する耐性変異の発現は認められませんでした。

■ベースライン時のHIV-1プロウイルスDNAにM184I/V変異が認められた患者におけるウイルス学的有効性(48週時・FAS-R)[副次評価項目]
ベースライン時のHIV-1プロウイルスDNAにM184I/V変異が認められ、かつ48週時のウイルス学的データがある患者においてウイルス学的有効性が検討されました。
48週時におけるHIV-1 RNA量<50 copies/mLの患者の割合は、イドビンソ®配合錠切替群で19/20例、ベースラインART継続群で4/4例でした。
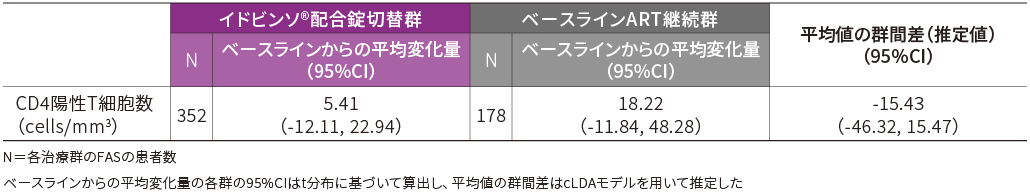
■免疫学的有効性(48週時・FAS)[副次評価項目]
48週時のCD4陽性T細胞数のベースラインからの平均変化量は以下の通りでした。
4.安全性
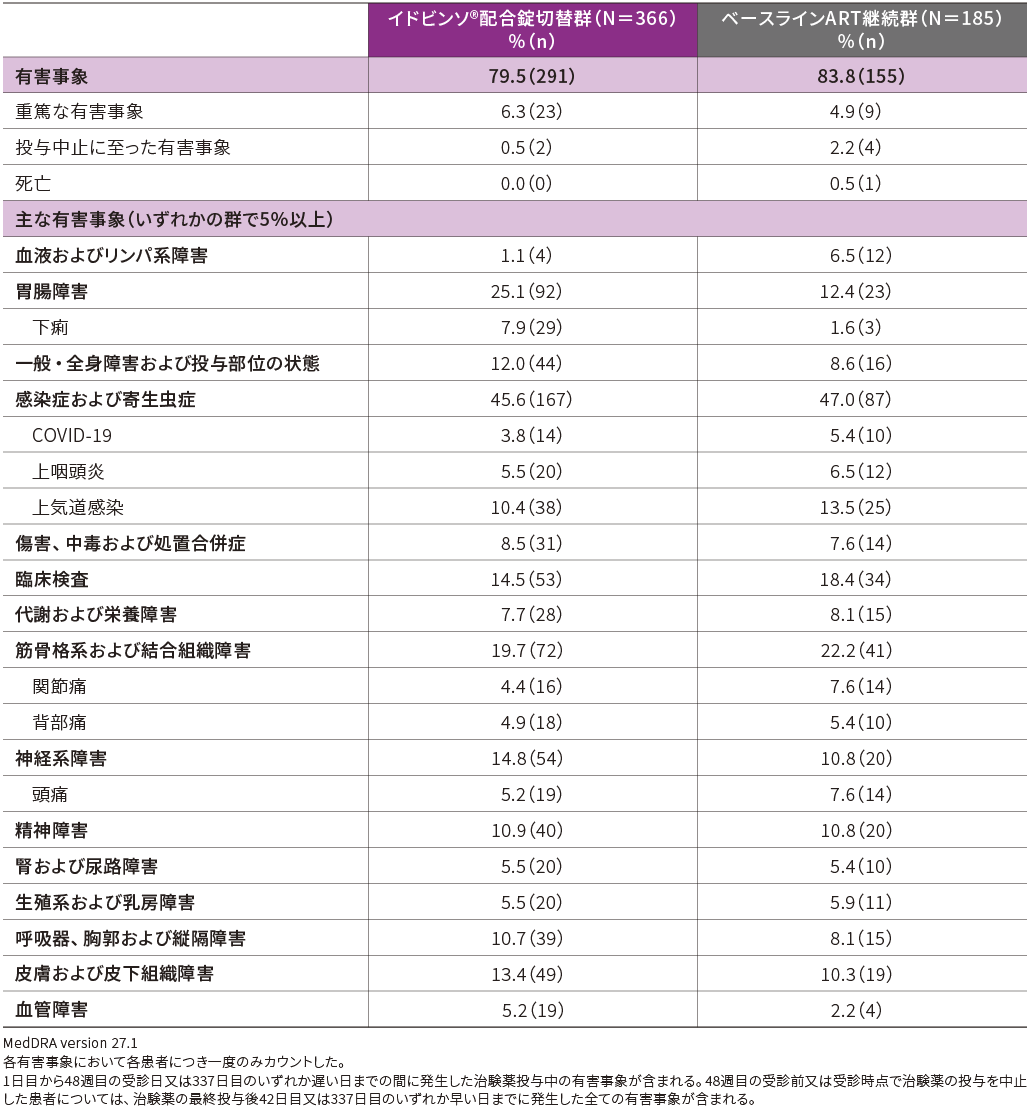
■有害事象(48週時・APaT)
主要評価項目である48週時までの有害事象発現率は、イドビンソ®配合錠切替群で79.5%(291/366例)、ベースラインART継続群で83.8%(155/185例)でした。
主な有害事象(いずれかの群で5%以上)は、下表の通りでした。
重篤な有害事象の発現率は、イドビンソ®配合錠切替群で6.3%(23/366例)、ベースラインART継続群で4.9%(9/185例)であり、その内訳は、イドビンソ®配合錠切替群で肺炎3例、心房細動2例、うっ血性心不全、腹痛、便秘、胃腸出血、胆石症、胃腸炎、骨髄炎、副鼻腔炎、脳振盪、腓骨骨折、頭部損傷、下肢骨折、手首関節骨折、トロポニンⅠ増加、コントロール不良の糖尿病、椎間板突出、カポジ肉腫、くも膜下出血、失神、自殺企図、蛋白尿、尿路閉塞、子宮頸部障害及び呼吸困難各1例(重複含む)であり、ベースラインART継続群で無顆粒球症、失血性貧血、蜂巣炎、ウイルス性上気道感染、靱帯断裂、半月板損傷、子宮頸部癌、浸潤性乳癌、肉腫、移行上皮癌、うつ病及び精神病性障害各1例でした。
投与中止に至った有害事象の発現率は、イドビンソ®配合錠切替群で0.5%(2/366例)、ベースラインART継続群で2.2%(4/185例)であり、その内訳は、イドビンソ®配合錠切替群で肺結核、下痢が各1例、ベースラインART継続群で無力症、肺結核、子宮頸部癌、精神病性障害が各1例でした。
死亡はベースラインART継続群で子宮頸部癌の1例に認められましたが治験薬との因果関係は否定されました。
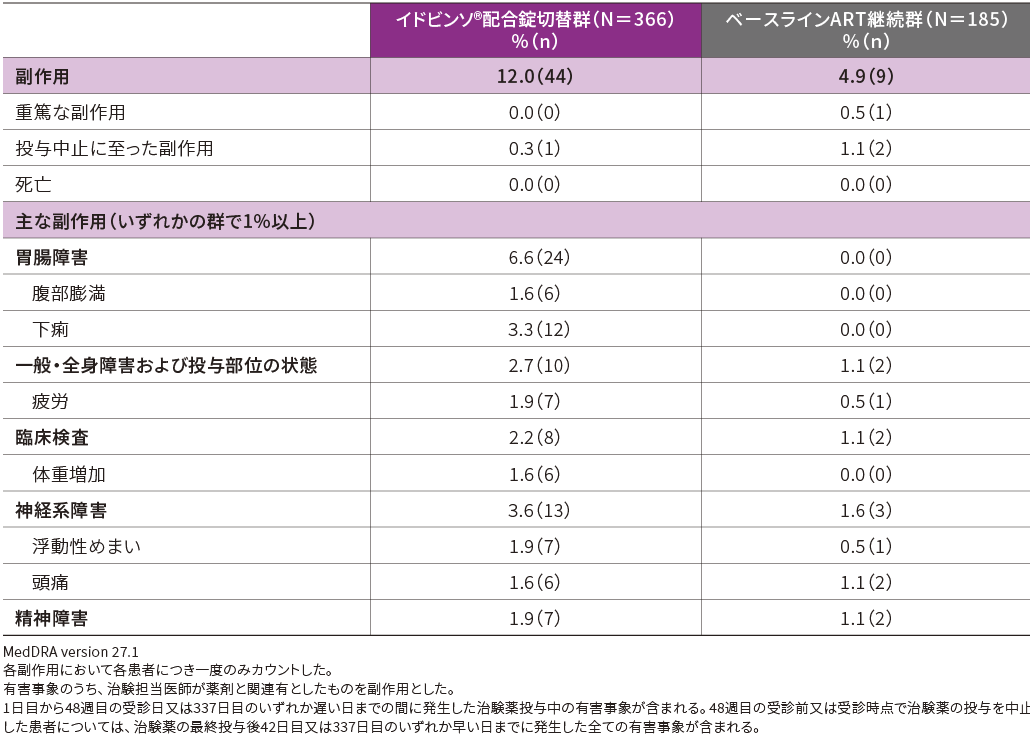
■副作用(48週時・APaT)
48週時までの副作用発現率は、イドビンソ®配合錠切替群で12.0%(44/366例)、ベースラインART継続群で4.9%(9/185例)でした。
主な副作用(いずれかの群で1%以上)は、イドビンソ®配合錠切替群で下痢3.3%(12/366例)、疲労及び浮動性めまい各1.9%(7/366例)、腹部膨満、体重増加、頭痛各1.6%(6/366例)、ベースラインART継続群で頭痛1.1%(2/185例)でした。
重篤な副作用は、ベースラインART継続群で精神病性障害1例でした。
投与中止に至った副作用は、イドビンソ®配合錠切替群で下痢が1例、ベースラインART継続群で無力症、精神病性障害が各1例でした。
両群ともに死亡例は認められませんでした。
副作用(48週時・APaT)
■腎機能への影響(48週時・APaT)[その他の重要な安全性評価項目]
eGFRのベースラインからの平均変化量

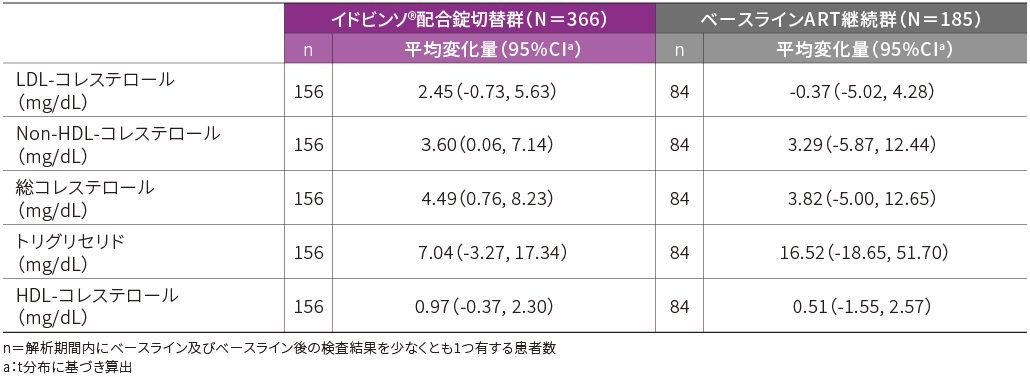
■脂質への影響(48週時・APaT)[その他の重要な安全性評価項目]
ベースラインARTにINSTIを含む患者(PI+INSTIレジメンを含まない)における空腹時脂質プロファイルの
ベースラインからの平均変化量(脂質低下薬服用患者を除く)
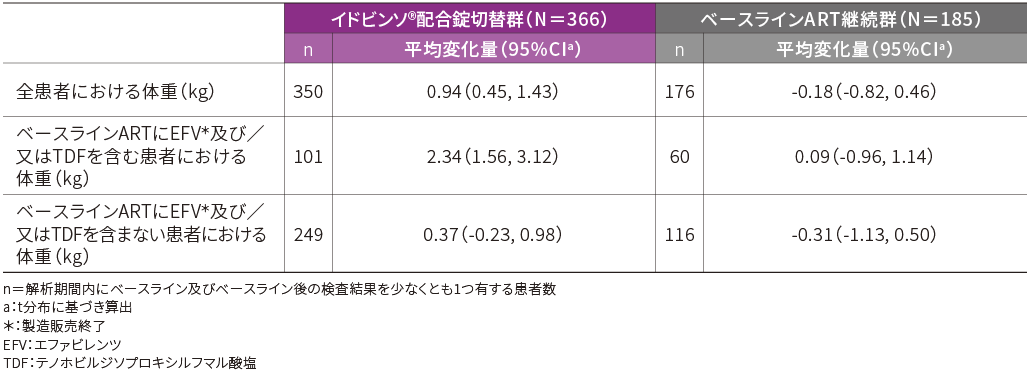
■体重への影響(48週時・APaT)[その他の重要な安全性評価項目]
体重のべースラインからの平均変化量
関連コンテンツ

イドビンソ®配合錠の作用機序
イドビンソ®配合錠の3つの作用機序について動画でご紹介します。ご監修:国立大学法人鹿児島大学 ヒトレトロウイルス学共同研究センター 抗ウイルス療法研究分野 教授 […]
製品基本Q&A
イドビンソ®・感染症関連領域情報

5学会による新型コロナウイルス感染症 診療の指針のポイント
こちらの動画では、5学会による新型コロナウイルス感染症 診療の指針のポイントについてご紹介します。

イドビンソ®配合錠の作用機序
イドビンソ®配合錠の3つの作用機序について動画でご紹介します。ご監修:国立大学法人鹿児島大学 ヒトレトロウイルス学共同研究センター 抗ウイルス療法研究分野 教授 […]

同種造血幹細胞移植後の晩期CMV再活性化リスクとプレバイミス®によるCMV感染管理
同種造血幹細胞移植後の晩期CMV再活性化リスク、特にPTCy後のCMV感染管理についてプレバイミス®の有効性・安全性を含めて紹介しています。