警告・禁忌を含む注意事項等情報
警告・禁忌を含む注意事項等情報
「警告・禁忌を含む注意事項等情報」の改訂に十分ご留意ください。
1. 警告
本剤の投与にあたっては、緊急時に十分対応できる医療施設において、がん化学療法に十分な知識・経験を持つ医師のもとで、本剤の投与が適切と判断される症例についてのみ実施すること。また、治療開始に先立ち、患者又はその家族に有効性及び危険性を十分説明し、同意を得てから投与すること。
2. 禁忌(次の患者には投与しないこと)
2.1 本剤の成分に対し過敏症の既往歴のある患者
2.2 重度の肝障害患者[9.3.1、16.6.1、17.3.1参照]
8. 重要な基本的注意
8.1 脱水症状があらわれることがあるので、必要に応じて、補液、電解質補充等を行うこと。また、投与にあたっては、患者に、脱水の兆候や脱水を避けるための注意点を指導すること。過度の嘔吐、下痢等が認められた場合には、医師の診察を受けるよう患者を指導すること。[11.1.4参照]
8.2 高血糖があらわれることがあるので、投与開始前及び投与開始後は定期的に血糖値の測定を行うこと。また、本剤の投与を開始する前に血糖値を適切にコントロールしておくこと。[9.1.2、11.1.5参照]
8.3 血小板減少、貧血、腎機能障害等があらわれることがあるので、本剤投与中は定期的に、血液検査(血球数算定、電解質/血清クレアチニンを含む血液生化学検査)を行うこと。[11.1.2、11.1.3、11.1.6参照]
9. 特定の背景を有する患者に関する注意
9.1 合併症・既往歴等のある患者
9.1.1 静脈血栓塞栓症を有する又は既往歴のある患者
肺塞栓症、深部静脈血栓症が発現、悪化するおそれがある。[11.1.1参照]
9.1.2 糖尿病又はその疑いのある患者
糖尿病が悪化するおそれがある。[8.2、11.1.5参照]
9.3 肝機能障害患者
本剤の血清中濃度が上昇するおそれがある。
9.3.1 重度の肝障害患者
投与しないこと。副作用が強くあらわれるおそれがある。[2.2、16.6.1、17.3.1参照]
9.3.2 軽度及び中等度の肝障害患者[7.3、16.6.1、17.3.1参照]
9.4.1 妊娠する可能性のある女性には、本剤投与中及び最終投与後6ヵ月間において避妊する必要性及び適切な避妊法について説明すること。[9.5、15.2 参照]
9.4.2 男性には、本剤投与中及び最終投与後3ヵ月間においてバリア法(コンドーム)を用いて避妊する必要性について説明すること。[15.2 参照]
9.5 妊婦
妊婦又は妊娠している可能性のある女性には、治療上の有益性が危険性を上回ると判断される場合にのみ投与すること。やむを得ず投与する場合には、本剤投与によるリスクについて患者に十分説明すること。動物実験では、ラット受胎能試験において本剤投与に関連した黄体数の増加が報告され、ラットの受胎能試験及び胚・胎児発生に関する試験において胚致死作用が報告されている。また、ウサギ及びラットの胚・胎児発生に関する試験及びトキシコキネティクス試験において、本剤の胎盤通過、生存胎児の平均体重の減少、骨化遅延及び骨格変異が報告されている。[9.4.1参照]
9.6 授乳婦
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討すること。本剤がヒト乳汁中へ移行するかは不明である。
9.7 小児等
小児等を対象とした臨床試験は実施していない。
9.8 高齢者
患者の状態を観察しながら慎重に投与すること。一般に生理機能が低下していることが多い。
11. 副作用
次の副作用があらわれることがあるので、観察を十分に行い、異常が認められた場合には投与を中止するなど適切な処置を行うこと。
11.1 重大な副作用
11.1.1 肺塞栓症(4.7%)、深部静脈血栓症(1.2%)
[9.1.1参照]
11.1.2 血小板減少症(25.6%)
[8.3参照]
11.1.3 貧血(12.8%)
[8.3参照]
11.1.4 脱水症状(1.2%)
[8.1参照]
11.1.5 高血糖(4.7%)
[8.2、9.1.2参照]
11.1.6 腎不全(頻度不明*)
[8.3参照]
11.2 その他の副作用
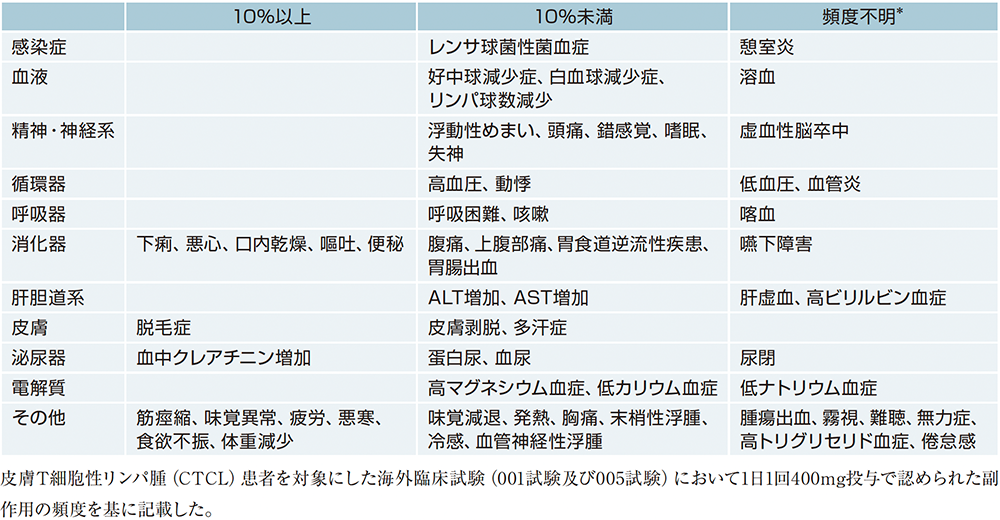
*:CTCL患者を対象にした国内臨床試験(089試験、1日1回400mg投与)、CTCL以外の患者を対象にした海外臨床試験及びCTCL患者を対象にした海外臨床試験(001試験及び005試験)において1日1回400mg投与以外で認められた副作用
14. 適用上の注意
14.1 薬剤交付時の注意
PTP包装の薬剤はPTPシートから取り出して服用するよう指導すること。PTPシートの誤飲により、硬い鋭角部が食道粘膜へ刺入し、更には穿孔を起こして縦隔洞炎等の重篤な合併症を併発することがある。
14.2 薬剤投与時の注意
カプセルを開けたり、つぶしたりしないこと。カプセル内の粉末を皮膚又は粘膜に直接接触させないこと。直接接触した場合には、完全に洗い流すこと。
15. その他の注意
15.2 非臨床試験に基づく情報
本剤のがん原性試験は実施していない。本剤は、細菌を用いた復帰突然変異試験(Ames試験)においてin vitroで変異原性を示し、チャイニーズハムスター卵巣(CHO)細胞に対してin vitroで染色体異常を誘発した。また、マウスへの本剤の投与により小核を有する赤血球の発現数を増加させた(マウス小核試験)。[9.4.1、9.4.2参照]
関連コンテンツ
